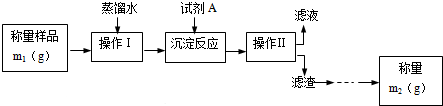
15.表为元素周期表的一部分,X、Y、Z、W、R为短周期元素,其中Z元素的原子最外层电子数是其内层电子数的3倍.下列说法正确的是( )
| X | Y | Z | |
| R | W | ||
| T |
| A. | 简单离子半径大小关系为:W>R>Z>Y | |
| B. | X有多种同素异形体,而Z不存在同素异形体 | |
| C. | R2W3可用RCl3溶液与Na2W溶液混合制取 | |
| D. | T的单质既能与盐酸反应又能与NaOH溶液反应 |
14.下列说法不正确的是( )
| A. | 屠呦呦女士用乙醚从黄花蒿中提取出青蒿素,该技术应用了萃取原理 | |
| B. | 解释化学反应速率理论有碰撞理论和过渡态理论,其中过渡态理论可解释温度、催化剂等因素对化学反应速率的影响 | |
| C. | 离子交换膜在工业上应用广泛,如氯碱工业使用阳离子交换膜 | |
| D. | 用氨水法处理燃煤烟气中的二氧化硫,既可消除其污染,又可得到副产品硫酸铵 |
7.NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有:Cu、Fe、Cr等杂质)为原料获得.工艺流程如图:

已知:25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表所示.
注:NiCO3是一种不溶于水易溶于强酸的沉淀.
请回答下列问题:
(1)下列措施可行,且能提高废渣浸出率的有AC.
A.升高反应温度 B.增大压强 C.在反应过程中不断搅拌
(2)在滤液Ⅰ中加入6%的H2O2,其作用是2Fe2++H2O2+2H+=2Fe3++2H2O(用离子方程式表示);加入H2O2后要保温一段时间且温度不宜太高的目的是加快氧化的速率,同时防止H2O2的分解;加入NaOH调节pH的范围是[5.6,8.4),为了除去溶液中的Fe3+、Cr3+离子.
(3)滤液Ⅱ的主要成分是Na2SO4、NiSO4.
(4)检验Ni2+已完全沉淀的实验方法是静置后向上层清液中再加入Na2CO3溶液后没有沉淀生成.
(5)操作Ⅰ的实验步骤依次为:
①过滤,并用蒸馏水洗涤沉淀2~3次直至流出液用pH试纸检验呈中性;
②向沉淀中滴加稀H2SO4,直至恰好完全溶解;
③蒸发浓缩、冷却结晶,过滤得NiSO4•6H2O晶体;
④用少量乙醇洗涤NiSO4•6H2O晶体并晾干.
0 153717 153725 153731 153735 153741 153743 153747 153753 153755 153761 153767 153771 153773 153777 153783 153785 153791 153795 153797 153801 153803 153807 153809 153811 153812 153813 153815 153816 153817 153819 153821 153825 153827 153831 153833 153837 153843 153845 153851 153855 153857 153861 153867 153873 153875 153881 153885 153887 153893 153897 153903 153911 203614

已知:25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表所示.
| Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
| Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 | 6.5×10-18 |
| 完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
请回答下列问题:
(1)下列措施可行,且能提高废渣浸出率的有AC.
A.升高反应温度 B.增大压强 C.在反应过程中不断搅拌
(2)在滤液Ⅰ中加入6%的H2O2,其作用是2Fe2++H2O2+2H+=2Fe3++2H2O(用离子方程式表示);加入H2O2后要保温一段时间且温度不宜太高的目的是加快氧化的速率,同时防止H2O2的分解;加入NaOH调节pH的范围是[5.6,8.4),为了除去溶液中的Fe3+、Cr3+离子.
(3)滤液Ⅱ的主要成分是Na2SO4、NiSO4.
(4)检验Ni2+已完全沉淀的实验方法是静置后向上层清液中再加入Na2CO3溶液后没有沉淀生成.
(5)操作Ⅰ的实验步骤依次为:
①过滤,并用蒸馏水洗涤沉淀2~3次直至流出液用pH试纸检验呈中性;
②向沉淀中滴加稀H2SO4,直至恰好完全溶解;
③蒸发浓缩、冷却结晶,过滤得NiSO4•6H2O晶体;
④用少量乙醇洗涤NiSO4•6H2O晶体并晾干.
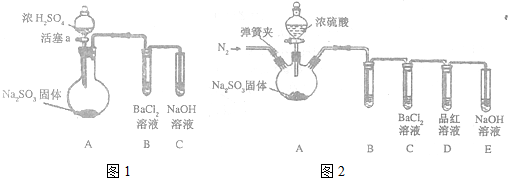
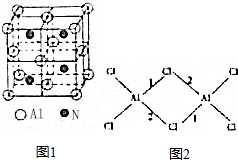
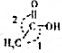 ,CH3COOH分子中σ键与π键个数之比7:1,分子中键角1<键角2(填“>”、“=”或“<”).
,CH3COOH分子中σ键与π键个数之比7:1,分子中键角1<键角2(填“>”、“=”或“<”).