1.下列分类正确的是( )
| A. | 酸:CH3COOH、H2SO3、NaHCO3、HF | B. | 碱:Cu2(OH)2CO3、NaOH、Fe(OH)2、Mg(OH)2 | ||
| C. | 盐:AgCl、BaSO4、NaH2PO4、Mg(NO3)2 | D. | 酸性氧化物:CO、CO2、SO2 SO3 |
18.化学是你,化学是我,化学深人我们生活,下列说法正确的是( )
| A. | 食用花生油、鸡蛋清和葡萄糖都能发生水解反应 | |
| B. | 木材纤维和土豆淀粉遇碘水均显蓝色 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都含有不饱和碳碳双键 | |
| D. | 加工后具有吸水性的植物纤维可用作食品干燥剂 |
16. 甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
ⅠCO(g)+2H2(g)?CH3OH(g)△H1
ⅡCO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2=-58kJ/mol
ⅢCO2(g)+H2(g)?CO(g)+H2O(g)△H3
回答下列问题:
(1)物质的标准生成热是常用的化学热力学数据,可以用来计算化学反应热.即化学反应热:△H=生成物标准生成热综合-反应物标准生成热总和.
已知四种物质的标准生成热如表:
A.计算△H1=-90.73kJ/molkJ/mol B.△H3>0(填=、<、>)
(2)由甲醇在一定条件下制备甲醚.一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g).实验数据见表:
下列说法正确的是AD
A.该反应的正反应为放热反应
B.达到平衡时,容器a中的CH3OH体积分数比容器b中的小
C.容器a中反应到达平衡所需时间比容器c中的长
D.若起始时向容器a中充入CH3OH 0.15mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
(3)合成气的组成$\frac{n({H}_{2})}{n(CO+C{O}_{2})}$=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图所示.
①α(CO)值随温度升高而减小(填“增大”或“减小”),其原因是升高温度时,反应Ⅰ为放热反应,平衡向左移动,使得体系中CO的量增大;反应Ⅲ为吸热反应,平衡向右移动,CO产生的量也增大;总结果,随温度升高,使CO的转化率降低.
②图中P1、P2、P3的大小关系为P3>P2>P1,其判断理由是相同温度下,由于反应Ⅰ为气体分子数减小的反应,加压有利于提升CO的转化率;而反应Ⅲ为气体分子数不变的反应,产生CO的量不受压强影响;故增大压强,CO的转化率升高.
(4)甲醇可以制成燃料电池,与合成气制成燃料电池相比优点是:装置简单,减小了电池的体积;若以硫酸作为电解质其负极反应为:CH3OH-6e-+H2O=CO2+6H+.
 甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:ⅠCO(g)+2H2(g)?CH3OH(g)△H1
ⅡCO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2=-58kJ/mol
ⅢCO2(g)+H2(g)?CO(g)+H2O(g)△H3
回答下列问题:
(1)物质的标准生成热是常用的化学热力学数据,可以用来计算化学反应热.即化学反应热:△H=生成物标准生成热综合-反应物标准生成热总和.
已知四种物质的标准生成热如表:
| 物质 | CO | CO2 | H2 | CH3OH(g) |
| 标准生成热(kJ/mol) | -110.52 | -393.51 | 0 | -201.25 |
(2)由甲醇在一定条件下制备甲醚.一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g).实验数据见表:
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |||
| CH3OH(g) | CH3OCH3(g) | H2O(g) | CH3OCH3(g) | H2O(g) | ||
| a | 387 | 0.20 | 0 | 0 | 0.080 | 0.080 |
| b | 387 | 0.40 | 0 | 0 | ||
| c | 207 | 0.20 | 0 | 0 | 0.090 | 0.090 |
A.该反应的正反应为放热反应
B.达到平衡时,容器a中的CH3OH体积分数比容器b中的小
C.容器a中反应到达平衡所需时间比容器c中的长
D.若起始时向容器a中充入CH3OH 0.15mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
(3)合成气的组成$\frac{n({H}_{2})}{n(CO+C{O}_{2})}$=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图所示.
①α(CO)值随温度升高而减小(填“增大”或“减小”),其原因是升高温度时,反应Ⅰ为放热反应,平衡向左移动,使得体系中CO的量增大;反应Ⅲ为吸热反应,平衡向右移动,CO产生的量也增大;总结果,随温度升高,使CO的转化率降低.
②图中P1、P2、P3的大小关系为P3>P2>P1,其判断理由是相同温度下,由于反应Ⅰ为气体分子数减小的反应,加压有利于提升CO的转化率;而反应Ⅲ为气体分子数不变的反应,产生CO的量不受压强影响;故增大压强,CO的转化率升高.
(4)甲醇可以制成燃料电池,与合成气制成燃料电池相比优点是:装置简单,减小了电池的体积;若以硫酸作为电解质其负极反应为:CH3OH-6e-+H2O=CO2+6H+.
14.将一定质量的镁、铜合金加入到稀硝酸中,合金完全溶解,假设反应过程中还原产物全部是NO,向所得溶液中加入物质的量浓度为3mol/L的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述正确的是( )
| A. | 反应中转移电子的总数为0.3mol | |
| B. | 反应过程中,消耗硝酸的物质的量为0.3mol | |
| C. | 沉淀完全时消耗NaOH溶液的体积为100mL | |
| D. | 开始加入合金的质量可能为3.4g |
13.下列溶液中微粒浓度关系一定正确的是( )
0 153606 153614 153620 153624 153630 153632 153636 153642 153644 153650 153656 153660 153662 153666 153672 153674 153680 153684 153686 153690 153692 153696 153698 153700 153701 153702 153704 153705 153706 153708 153710 153714 153716 153720 153722 153726 153732 153734 153740 153744 153746 153750 153756 153762 153764 153770 153774 153776 153782 153786 153792 153800 203614
| A. | 0.1mol/L的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) | |
| B. | 室温下,pH=7的醋酸和醋酸钠的混合溶液中:c(CH3COO-)>c(Na+) | |
| C. | 将水加热到100℃,pH=6:c(H+)>c(OH-) | |
| D. | 同浓度的三种溶液:①CH3COONH4 ②NH4Cl ③NH3•H2O中,c(NH4+)由大到小的顺序是②③① |
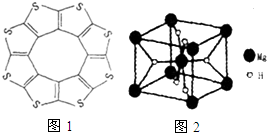 氢能被视为21世纪最具发展潜力的清洁能源.
氢能被视为21世纪最具发展潜力的清洁能源.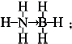 ;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).
;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式). 布洛芬具有解热镇痛作用,常规剂量使用时,不良反应发生率低,是国内外包括世界卫生组织公认的用于小儿发热的经典解热镇痛药.布洛芬的结构简式如图:
布洛芬具有解热镇痛作用,常规剂量使用时,不良反应发生率低,是国内外包括世界卫生组织公认的用于小儿发热的经典解热镇痛药.布洛芬的结构简式如图: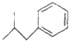 $→_{AlCl_{3}}^{CH_{3}COCl}$A$\stackrel{H_{2}}{→}$
$→_{AlCl_{3}}^{CH_{3}COCl}$A$\stackrel{H_{2}}{→}$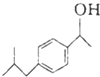 $\stackrel{CO}{→}$布洛芬
$\stackrel{CO}{→}$布洛芬 +
+ $\stackrel{AlCl_{3}}{→}$
$\stackrel{AlCl_{3}}{→}$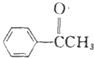 +HCl,请写出A的结构简式
+HCl,请写出A的结构简式

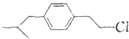 为原料合成布洛芬(用合成路线流程图表示;无机原料任选,并注明反应条件).
为原料合成布洛芬(用合成路线流程图表示;无机原料任选,并注明反应条件). .
. 可用键线式表示为
可用键线式表示为 ,
, 可用键线式表示为
可用键线式表示为 ;
; ;
;
 ;
; ;
; 结构
结构 .
. 制
制 的流程图并注明反应条件.
的流程图并注明反应条件.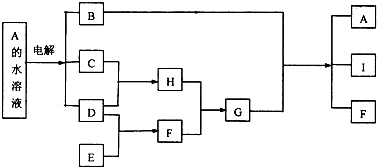
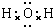 ;
;