12.已知化学反应A2(g)+B2(g)=2AB(s)的能量变化如图所示,下列叙述正确的是( )

| A. | 该反应为放热反应 | B. | 加催化剂能降低该反应焓变 | ||
| C. | A-B的键能为bkJ•mol-1 | D. | 该反应的反应热为△H=(a-b)kJ•mol-1 |
11.下列说法正确的是( )
| A. | 分子式为C5H12的有机物化学性质相似 | |
| B. | 相同条件下,等质量的甲烷按a、b两种途径完全转化,途径a比b放出更多热量 | |
| C. | 需加热才能发生的反应都是吸热反应 | |
| D. | 电镀时待镀金属作阳极,镀层金属作阴极 |
10.下列有关化学用语表示正确的是( )
| A. | CF4的电子式: | B. | 对甲基苯酚的结构简式: | ||
| C. | 甲酸甲酯的实验式:CH2O | D. | ${\;}_{8}^{16}$O2-离子的结构示意图: |
9.化学与生活、生产、环境等密切相关,下列叙述正确的是( )
| A. | 涤纶、塑料、光导纤维都是有机高分子材料 | |
| B. | 煤经过气化或液化等物理变化可转化为清洁燃料 | |
| C. | 用电镀厂的废水直接灌溉农田,可提高水的利用率 | |
| D. | 工业燃煤中加入适量生石灰,可减少酸雨的形成 |
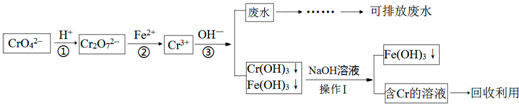
7.某化学兴趣小组设计如下方案测定饱和食盐水的电解率.
[提示:饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%]
方案一:连接图甲、乙装置,在洗气瓶a中盛放足量的氢氧化钠溶液,通过测定洗气瓶a在电解前后的质量变化来计算饱和食盐水的电解率.

(1)正确的连接顺序为导管口B(填“A”或“B”)连导管口C,若事先往甲装置的饱和食盐水中滴入酚酞,则电解过程甲装置中铁棒(填“铁棒”或“碳棒”)附近的溶液变红.
(2)电解饱和食盐水总反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
方案二:利用甲装置电解后的溶液,通过中和滴定来测定饱和食盐水的电解率.
(3)部分实验过程如下:
①用碱式滴定管(填“酸式滴定管”或“碱式滴定管”)量取10.00mL电解后的溶液,加入锥形瓶中;
②向锥形瓶中加入几滴酚酞试液,用0.2000mol•L-1标准盐酸滴定待测液,边滴边摇动锥形瓶,直到滴入最后一滴时,锥形瓶中溶液颜色由红色变无色,并保持半分钟不褪色时停止滴定;
③该小组所测实验数据如表:
未电解前饱和食盐水的物质的量浓度为5.4mol•L-1,经计算,求出该食盐水的电解率为7.4%.
④下列操作,会导致实验结果偏低的是AB(填序号).
A.滴定时锥形瓶中液滴飞溅出来
B.滴定前读数时平视,终点读数时俯视
C.锥形瓶用蒸馏水洗净后没用待测液润洗
D.酸式滴定管尖端气泡没有排除,滴定后消失.
[提示:饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%]
方案一:连接图甲、乙装置,在洗气瓶a中盛放足量的氢氧化钠溶液,通过测定洗气瓶a在电解前后的质量变化来计算饱和食盐水的电解率.

(1)正确的连接顺序为导管口B(填“A”或“B”)连导管口C,若事先往甲装置的饱和食盐水中滴入酚酞,则电解过程甲装置中铁棒(填“铁棒”或“碳棒”)附近的溶液变红.
(2)电解饱和食盐水总反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
方案二:利用甲装置电解后的溶液,通过中和滴定来测定饱和食盐水的电解率.
(3)部分实验过程如下:
①用碱式滴定管(填“酸式滴定管”或“碱式滴定管”)量取10.00mL电解后的溶液,加入锥形瓶中;
②向锥形瓶中加入几滴酚酞试液,用0.2000mol•L-1标准盐酸滴定待测液,边滴边摇动锥形瓶,直到滴入最后一滴时,锥形瓶中溶液颜色由红色变无色,并保持半分钟不褪色时停止滴定;
③该小组所测实验数据如表:
| 实验序号 | 盐酸体积(mL) |
| 第一组 | 19.90 |
| 第二组 | 24.70 |
| 第三组 | 20.10 |
| 第四组 | 20.00 |
④下列操作,会导致实验结果偏低的是AB(填序号).
A.滴定时锥形瓶中液滴飞溅出来
B.滴定前读数时平视,终点读数时俯视
C.锥形瓶用蒸馏水洗净后没用待测液润洗
D.酸式滴定管尖端气泡没有排除,滴定后消失.
4. 利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
已知:①CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.2kJ•mol-1
②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42.3kJ•mol-1
(1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=+163.9 kJ/mol.
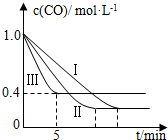
(2)为了探究反应条件对反应CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42.3kJ•mol-1的影响,某活动小组设计了三个实验,实验曲线如图所示.
①请依据实验曲线图补充完整表格中的实验条件:X=530℃,Y=5MPa.
②实验Ⅲ从开始至平衡,其平均反应速度率v (CO)=0.12mol•L-1•min-1.
③实验Ⅱ达平衡时CO的转化率大于 实验Ⅲ达平衡时CO的转化率(填“大于”、“小于”或“等于”).
④在530℃时,平衡常数K=1,若往1L容器中投入0.2mol CO(g)、0.2mol H2O(g)、1mol CO2(g)、0.1mol H2(g),此时化学反应将向逆方向(填“向正方向”、“向逆方向”或“不”) 移动.
 利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.已知:①CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206.2kJ•mol-1
②CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42.3kJ•mol-1
(1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=+163.9 kJ/mol.
(2)为了探究反应条件对反应CO(g)+H2O(g)?CO2(g)+H2(g)△H=-42.3kJ•mol-1的影响,某活动小组设计了三个实验,实验曲线如图所示.
| 编号 | 温度 | 压强 | c始(CO) | c始(H2O) |
| Ⅰ | 530℃ | 3MPa | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅱ | X | Y | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅲ | 630℃ | 5MPa | 1.0mol•L-1 | 3.0mol•L-1 |
②实验Ⅲ从开始至平衡,其平均反应速度率v (CO)=0.12mol•L-1•min-1.
③实验Ⅱ达平衡时CO的转化率大于 实验Ⅲ达平衡时CO的转化率(填“大于”、“小于”或“等于”).
④在530℃时,平衡常数K=1,若往1L容器中投入0.2mol CO(g)、0.2mol H2O(g)、1mol CO2(g)、0.1mol H2(g),此时化学反应将向逆方向(填“向正方向”、“向逆方向”或“不”) 移动.
3. 在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
0 153344 153352 153358 153362 153368 153370 153374 153380 153382 153388 153394 153398 153400 153404 153410 153412 153418 153422 153424 153428 153430 153434 153436 153438 153439 153440 153442 153443 153444 153446 153448 153452 153454 153458 153460 153464 153470 153472 153478 153482 153484 153488 153494 153500 153502 153508 153512 153514 153520 153524 153530 153538 203614
 在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | 反应温度:T1>T2 | B. | a、b两点的平衡常数:Kb>Ka | ||
| C. | a、c两点气体的颜色:a浅,c深 | D. | b、c两点的反应速率:v(b)>v(c) |