9.下列鉴别物质的方法能达到目的是( )
| A. | 用加热、称重的方法鉴别Na2CO3固体和NaHCO3固体 | |
| B. | 用焰色反应鉴别NaCl固体和NaOH固体 | |
| C. | 用KSCN溶液鉴别FeCl3溶液和Fe2(SO4)3溶液 | |
| D. | 检验未知溶液是否含SO42ˉ可先加氯化钡,再加稀盐酸 |
6.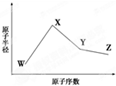 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
Ⅰ.(1)X位于元素周期表中的位置第三周期第ⅠA族;W的基态原子核外有2个未成对电子.
(2)X的单质和Y的单质相比,熔点较高的是Si(写化学式);Z的气态氢化物和溴化氢相比,较稳定的是HCl(写化学式).
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是SiCl4+4H2O=H4SiO4↓+4HCl.
Ⅱ.部分化学键的键能见下表:
(1)比较下列两组物质的熔点高低(填“>”“<”)SiC>Si SiCl4< SiO2
(2)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g),计算该反应的反应热△H=+236kJ•mol-1.
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.Ⅰ.(1)X位于元素周期表中的位置第三周期第ⅠA族;W的基态原子核外有2个未成对电子.
(2)X的单质和Y的单质相比,熔点较高的是Si(写化学式);Z的气态氢化物和溴化氢相比,较稳定的是HCl(写化学式).
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是SiCl4+4H2O=H4SiO4↓+4HCl.
Ⅱ.部分化学键的键能见下表:
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/ kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
(2)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g),计算该反应的反应热△H=+236kJ•mol-1.
5.有关溶液中所含离子的检验,下列判断正确的是( )
| A. | 加入硝酸酸化,再滴加KSCN溶液后有红色物质生成,则原溶液中一定有Fe3+存在 | |
| B. | 加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO32-存在 | |
| C. | 用某溶液做焰色反应实验时火焰为黄色,则该溶液中一定有钠元素,可能有钾元素 | |
| D. | 分别含有Mg2+、Fe3+、Al3+、Cu2+、Fe2+和Na+的六种盐溶液,只用NaOH溶液是不能一次鉴别开的 |
4.下表中对应关系正确的是( )
| A | CH3CH3+Cl2$\stackrel{光照}{→}$CH3CH2Cl+HCl CH2=CH2+HCl→CH3CH2Cl | 均为取代反应 |
| B | 由油脂得到甘油;由卤代烃制醇 | 均发生了水解反应 |
| C | Cl2+2Br?→2Cl?+Br2;Zn+Cu2+→Zn2++Cu | 均为单质被还原的置换反应 |
| D | 2Na2O2+2H2O→4NaOH+O2↑; 2F2+2H2O→4HF+O2 | 均为水作还原剂的氧化还原反应 |
| A. | A | B. | B | C. | C | D. | D |
2.下列有关说法中,正确的是( )
| A. | 气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气 | |
| B. | 碳酸钠可作为治疗胃酸过多的药物,食品发酵剂 | |
| C. | 通过丁达尔效应可以鉴别稀豆浆和氢氧化铁胶体 | |
| D. | 焰色反应一定伴随着化学变化和物理过程 |
17.在强酸性的溶液中能大量共存的离子组是( )
0 153238 153246 153252 153256 153262 153264 153268 153274 153276 153282 153288 153292 153294 153298 153304 153306 153312 153316 153318 153322 153324 153328 153330 153332 153333 153334 153336 153337 153338 153340 153342 153346 153348 153352 153354 153358 153364 153366 153372 153376 153378 153382 153388 153394 153396 153402 153406 153408 153414 153418 153424 153432 203614
| A. | Na+、Fe2+、SO32- | B. | Na+、K+、SO42- | C. | K+、SO42-、OH- | D. | Al3+、NO3-、S2- |
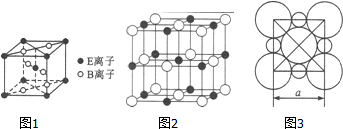 A、B、C、D、E五种常见元素的核电荷数依次增大.A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态3d轨道上有2个电子.请回答下列问题:
A、B、C、D、E五种常见元素的核电荷数依次增大.A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态3d轨道上有2个电子.请回答下列问题: A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大,A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,C与B同主族,D元素的价电子数是其余电子数的一半,E与D同族,F与A同主族,回答下列问题:
A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大,A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,C与B同主族,D元素的价电子数是其余电子数的一半,E与D同族,F与A同主族,回答下列问题: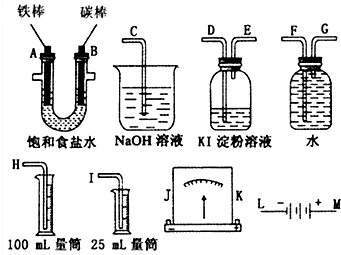 某课外小组做电解食盐水的探究实验,现有如图所示所列实验装置,请从其中选择适当的装置并加以组装,要求检验氯气的氧化性,并测定产生氢气的体积.
某课外小组做电解食盐水的探究实验,现有如图所示所列实验装置,请从其中选择适当的装置并加以组装,要求检验氯气的氧化性,并测定产生氢气的体积.