题目内容
9.下列鉴别物质的方法能达到目的是( )| A. | 用加热、称重的方法鉴别Na2CO3固体和NaHCO3固体 | |
| B. | 用焰色反应鉴别NaCl固体和NaOH固体 | |
| C. | 用KSCN溶液鉴别FeCl3溶液和Fe2(SO4)3溶液 | |
| D. | 检验未知溶液是否含SO42ˉ可先加氯化钡,再加稀盐酸 |
分析 A.碳酸钠加热不分解,而碳酸氢钠加热分解生成碳酸钠、二氧化碳气体和水;
B.氯化钠和氢氧化钠的焰色反应都是黄色;
C.氯化铁和硫酸铁都含有铁离子,滴入硫氰化钾溶液都显示红色;
D.应该先加入稀盐酸,排除干扰离子,再加入氯化钡溶液.
解答 解:A.碳酸氢钠加热分解,而碳酸钠不分解,可用加热、称重的方法鉴别Na2CO3固体和NaHCO3固体,故A正确;
B.NaCl固体和NaOH固体的焰色反应的火焰颜色都是黄色,无法用焰色反应鉴别,故B错误;
C.KSCN溶液分别滴入FeCl3溶液和Fe2(SO4)3溶液中,两溶液都显示红色,无法用硫氰化钾鉴别,故C错误;
D.先加入氯化钡溶液,生成的白色沉淀可能为氯化银,干扰了硫酸根离子的检验,应该先加入稀盐酸排除干扰离子,然后加入氯化钡溶液,故D错误;
故选A.
点评 本题考查了物质的检验和鉴别实验方案的设计,题目难度中等,明确常见物质的性质及检验方法为解答关键,注意设计检验方案时必须排除干扰情况,确保方案的严密性,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
16.X、Y、Z、W、M均为短周期元素,原子序数依次增加,X、M同一主族,Z+、W3+和Y2-的电子层结构相同,M是地壳中含量第二的非金属元素.下列说法正确的是( )
| A. | 原子最外层电子数:X>Y>Z | B. | 离子半径:W3+>Y2- | ||
| C. | 原子序数:X+M>Y+W | D. | 单质沸点:M>Z>Y |
14. 甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图.下列有关叙述不正确的是( )
甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图.下列有关叙述不正确的是( )
 甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图.下列有关叙述不正确的是( )
甲醇-空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图.下列有关叙述不正确的是( )| A. | H+从负极区通过交换膜移向正极区 | |
| B. | 正极的电极反应式为:O2+H2O+4e-═4OH- | |
| C. | 图中a、b、c、d物质分别是CO2、CH2OH、H2O | |
| D. | 用该燃料电池电解饱和食盐水,产生1.5mol氯气,需要消耗甲醇16克 |
4.下表中对应关系正确的是( )
| A | CH3CH3+Cl2$\stackrel{光照}{→}$CH3CH2Cl+HCl CH2=CH2+HCl→CH3CH2Cl | 均为取代反应 |
| B | 由油脂得到甘油;由卤代烃制醇 | 均发生了水解反应 |
| C | Cl2+2Br?→2Cl?+Br2;Zn+Cu2+→Zn2++Cu | 均为单质被还原的置换反应 |
| D | 2Na2O2+2H2O→4NaOH+O2↑; 2F2+2H2O→4HF+O2 | 均为水作还原剂的氧化还原反应 |
| A. | A | B. | B | C. | C | D. | D |
19.某课外活动小组设计的用化学电源使LED灯发光的装置如图.下列说法错误的是( )
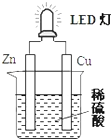

| A. | 铜片表面有气泡生成,锌片上发生氧化反应 | |
| B. | 如果将稀硫酸换成葡萄糖溶液,不能使LED灯发光 | |
| C. | 装置中存在“化学能→电能→光能”的转换 | |
| D. | 如果将铜片换成铁片,则锌片为正极 |
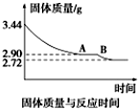 煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题: