4.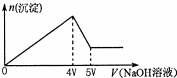 向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )
向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )
 向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )
向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )| A. | 1:2 | B. | 1:1 | C. | 2:3 | D. | 3:2 |
3.为提纯下列物质(括号内为杂质),所选用的试剂和分离方法均正确的是( )
| 选项 | 物质 | 除杂试剂 | 分离方法 |
| A | NaCl溶液(CuCl2) | 钠 | 结晶 |
| B | S02(SO3) | NaOH溶液 | 萃取 |
| C | Cu(NO3)2溶液(AgNO3) | 铜粉 | 分液 |
| D | 乙醇(水) | … | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
2.下列有关实验现象的描述中,正确的是( )
| A. | 氢气在氯气中燃烧,产生大量白烟 | |
| B. | 钠在空气中燃烧,最终得到白色固体 | |
| C. | 向硅酸钠溶液中滴加稀盐酸,产生白色胶状物 | |
| D. | 向氯化铝溶液中滴加氨水,先产生白色沉淀,后沉淀消失 |
1.下列离子方程式书写正确的是( )
| A. | 碳酸钙与稀盐酸反应CO32-+2H+═CO2↑+H2O | |
| B. | 稀硫酸与氯化钡溶液反应Ba2++SO42-═BaSO4 | |
| C. | 氢氧化镁与稀硫酸反应OH--+H+═H2O | |
| D. | 铁钉放入硫酸铜溶液中2Fe+3Cu2+═2Fe3++3Cu |
20.铁粉和水蒸气反应的装置如图所示,有关该反应的说法正确的是( )


| A. | 该反应属于复分解反应 | |
| B. | 网罩的作用是集中火焰,提高温度 | |
| C. | 湿棉花的作用是给试管降温,防止炸裂 | |
| D. | 反应中水既不是氧化剂,也不是还原剂 |
19.C60自被发现以来,已逐步应用到超导、材料等各个领域.下列有关说法正确的是( )

| A. | C60就是金刚石 | B. | C60属于有机化合物 | ||
| C. | C60的摩尔质量是720g/mol | D. | 1mol C60完全燃烧生成22.4L CO2 |
18.某无色透明的溶液中,能大量共存的离子组是( )
| A. | Na+、Cu2+、SO42-、OH- | B. | K+、Ba2+、Cl-、NO3- | ||
| C. | K+、Ca2+、Cl-、MnO4- | D. | Na+、CO32-、SO42-、H+ |
17.下列做法正确的是( )
| A. | 金属钠着火,立即用水扑灭 | |
| B. | 稀释浓硫酸时,将水倒入浓硫酸中 | |
| C. | 在量筒中配置100mL,1mol/L NaCl溶液 | |
| D. | 大量氯气泄漏时,尽量沿高处迅速离开现场 |
16.铬(Cr)有多种化合物,在工业生产中有广泛的用途.
(1)工业上利用铬铁矿(FeO Cr2O3)冶炼铬的工艺流程如下:
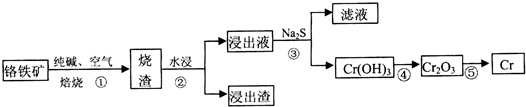 a.操作①中为加热焙烧速率和提高原料的利用率,可采取的措施是将铬铁矿粉碎(答一条即可).
a.操作①中为加热焙烧速率和提高原料的利用率,可采取的措施是将铬铁矿粉碎(答一条即可).
b.浸出液中含有的主要成分为Na2CrO4,向滤液中加酸化的氯化钡溶液有白色沉淀生成,则操作③发生反应的离子方程式CrO42-+Ba2+=BaCrO4↓.
(2)铬的化合物有毒,排放前要经过处理,通常用电解法:
将含Cr2O72-的废水放入电解槽内,加入一定量氯化钠,用铁作电极提供Fe2+,Cr2O72-将Fe2+氧化生成Fe3+,本身被还原生成Cr3+,最后Cr3+和Fe3+以Cr(OH)3和Fe(OH)3的形式除去.铁作电解槽的阳极,阴极反应式为2H++2e-=H2↑,Cr2O72-氧化Fe2+的离子方程式为6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O.
(3)CrO3是一种常见的铬的氧化物,其热稳定性较差,加热时逐步分解.取100gCrO3加热,剩余固体的质量随温度的变化如下表所示.
则x=84.00,y为Cr2O5(写化学式).
0 153201 153209 153215 153219 153225 153227 153231 153237 153239 153245 153251 153255 153257 153261 153267 153269 153275 153279 153281 153285 153287 153291 153293 153295 153296 153297 153299 153300 153301 153303 153305 153309 153311 153315 153317 153321 153327 153329 153335 153339 153341 153345 153351 153357 153359 153365 153369 153371 153377 153381 153387 153395 203614
(1)工业上利用铬铁矿(FeO Cr2O3)冶炼铬的工艺流程如下:
 a.操作①中为加热焙烧速率和提高原料的利用率,可采取的措施是将铬铁矿粉碎(答一条即可).
a.操作①中为加热焙烧速率和提高原料的利用率,可采取的措施是将铬铁矿粉碎(答一条即可).b.浸出液中含有的主要成分为Na2CrO4,向滤液中加酸化的氯化钡溶液有白色沉淀生成,则操作③发生反应的离子方程式CrO42-+Ba2+=BaCrO4↓.
(2)铬的化合物有毒,排放前要经过处理,通常用电解法:
将含Cr2O72-的废水放入电解槽内,加入一定量氯化钠,用铁作电极提供Fe2+,Cr2O72-将Fe2+氧化生成Fe3+,本身被还原生成Cr3+,最后Cr3+和Fe3+以Cr(OH)3和Fe(OH)3的形式除去.铁作电解槽的阳极,阴极反应式为2H++2e-=H2↑,Cr2O72-氧化Fe2+的离子方程式为6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O.
(3)CrO3是一种常见的铬的氧化物,其热稳定性较差,加热时逐步分解.取100gCrO3加热,剩余固体的质量随温度的变化如下表所示.
| 温度/K | 480 | 505 | 615 | 730 |
| 质量/g | 94.67 | 92.00 | x | 76.00 |
| 化学式 | Cr3O8 | y | CrO2 | Cr2O3 |