5.由软锰矿制备高锰酸钾的主要反应如下:
熔融氧化 3MnO2+KClO3+6KOH $\stackrel{高温}{→}$3K2MnO4+KCl+3H2O
加酸歧化 3K2MnO4+2CO2→2KMnO4+MnO2↓+2K2CO3
已知相关物质的溶解度(20℃)
完成下列填空:
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和cd.(填序号)
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.泥三角
(2)在“加酸岐化”时不宜用硫酸的原因是生成K2SO4溶解度小,会降低产品的纯度;不宜用盐酸的原因是盐酸具有还原性,会被氧化,降低产品的量.
反应之后得到高锰酸钾的步骤是:过滤、蒸发结晶、趁热过滤.
该步骤能够得到高锰酸钾的原理是KMnO4和K2CO3的溶解度不同.
(3)采用电解法也可实现K2MnO4的转化,2K2MnO4+2H2O$\stackrel{通电}{→}$ 2KMnO4+2KOH+H2↑.与原方法相比,电解法的优势为 K2MnO4中的锰元素可以完全转化到KMnO4中,原子利用率高.
熔融氧化 3MnO2+KClO3+6KOH $\stackrel{高温}{→}$3K2MnO4+KCl+3H2O
加酸歧化 3K2MnO4+2CO2→2KMnO4+MnO2↓+2K2CO3
已知相关物质的溶解度(20℃)
| 物质 | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| 溶解度g/100g | 111 | 33.7 | 11.1 | 6.34 |
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和cd.(填序号)
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.泥三角
(2)在“加酸岐化”时不宜用硫酸的原因是生成K2SO4溶解度小,会降低产品的纯度;不宜用盐酸的原因是盐酸具有还原性,会被氧化,降低产品的量.
反应之后得到高锰酸钾的步骤是:过滤、蒸发结晶、趁热过滤.
该步骤能够得到高锰酸钾的原理是KMnO4和K2CO3的溶解度不同.
(3)采用电解法也可实现K2MnO4的转化,2K2MnO4+2H2O$\stackrel{通电}{→}$ 2KMnO4+2KOH+H2↑.与原方法相比,电解法的优势为 K2MnO4中的锰元素可以完全转化到KMnO4中,原子利用率高.
20.下列叙述不正确的是( )
| A. | 锌跟稀硫酸反应制取氢气,加入少量的硫酸铜能加快反应速率 | |
| B. | 镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀 | |
| C. | 钢铁表面常易被锈蚀生成Fe2O3•nH2O | |
| D. | 钢铁在发生析氢腐蚀和吸氧腐蚀时,电极反应相同的是负极反应 |
18.下表中实验操作能达到实验目的是( )
| 实验操作 | 实验目的 | |
| A | 向甲酸钠溶液中加新制的Cu(OH)2并加热 | 确定甲酸钠具有醛基性质 |
| B | 苯中有少量苯酚,加入氢氧化钠溶液后,分液 | 除去苯中混有的苯酚 |
| C | 向酒精和水的混合溶液中加入金属钠 | 确定酒精中混有水 |
| D | 将氯乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验水解产物中的氯离子 |
| A. | A | B. | B | C. | C | D. | D |
17.下列有机物的系统命名中正确的是( )
| A. | 3-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 3-甲基-5-己烯 | D. | 3,3-二甲基-1-戊烯 |
16.下图所示的实验操作与方法正确的是( )
0 152821 152829 152835 152839 152845 152847 152851 152857 152859 152865 152871 152875 152877 152881 152887 152889 152895 152899 152901 152905 152907 152911 152913 152915 152916 152917 152919 152920 152921 152923 152925 152929 152931 152935 152937 152941 152947 152949 152955 152959 152961 152965 152971 152977 152979 152985 152989 152991 152997 153001 153007 153015 203614
| A. |  检验装置气密性 | B. |  过滤 | C. |  点燃酒精灯 | D. |  称量氯化钠 |

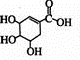 +Br2→
+Br2→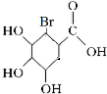 .
. +H2O→
+H2O→ +CH3COOH.
+CH3COOH.

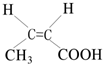 .
. .
.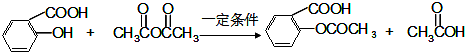 .
.