15.手性分子是指在分子结构 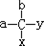 中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
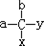 中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )| A. | 苹果酸: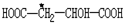 | B. | 丙氨酸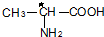 | C. | 葡萄糖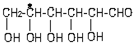 | D. | 甘油醛 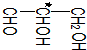 |
14.根据下列事实得出的结论正确的是( )
| A. | 试样$→_{水浴加热}^{银氨溶液}$产生银镜结论:该试样是醛类 | |
| B. | 某卤代烃试样$→_{加热}^{氢氧化钠溶液}$$\stackrel{滴入硝酸银溶液}{→}$最终的沉淀不是白色.结论:该卤代烃中不含氯原子 | |
| C. | 某溶液$\stackrel{打开瓶盖}{→}$冒着白雾$\stackrel{用蘸有浓氨水玻璃棒}{→}$产生大量白烟,结论:此溶液为浓盐酸 | |
| D. | 无色溶液$\stackrel{焰色反应}{→}$呈黄色:结论:此溶液一定含有钠元素 |
13.下列各化合物的命名中正确的是( )
| A. | CH2=CH-CH=CH2 1,3-二丁烯 | B. |  2-甲基丁烷 2-甲基丁烷 | ||
| C. |  甲基苯酚 甲基苯酚 | D. |  3-丁醇 3-丁醇 |
9.下列判断正确的是( )
| A. | 同体积、同浓度的NaF和NaCl溶液中,所有离子总数,N(NaCl)>N(NaF);同体积同浓度的Na2CO3和Na2SO4溶液中,所有离子总数,N(Na2CO3)>N(Na2SO4) | |||||||||||
| B. | 以下是某温度下高氯酸、硫酸、硝酸和盐酸在冰醋酸中的电离常数,则在冰醋酸中硫酸的电离方程式可表示为H2SO4?2H++SO42-
| |||||||||||
| C. | 已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,[c(Na+)-c(F-)]<[c(K+)-c(CH3COO-)] | |||||||||||
| D. | 平衡体系CaCO3(s)?CaO(s)+CO2中仅含有碳酸钙、氧化钙及二氧化碳气体.某时刻,保持温度不变,将容器体积缩小为原来的一半并保持不变,则二氧化碳浓度增大 |
8.下列说法正确的是( )
| A. | 乙烯能使溴水、酸性高锰酸钾溶液褪色,其反应类型相同 | |
| B. | 某烷烃R的相对分子质量为86,其氯代物只有2种,则R的名称一定为2,3-二甲基丁烷 | |
| C. | 若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物只有CHCl3 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
7.X、Y、Z是原子序数依次增大且属于不同周期的三种常见短周期元素.三种元素相互之间可以形成1:1型的化合物M、N、R,常温下M、N为固体,R为液体.M、N遇到水都能产生气体,而且产生的气体相互可以化合,下列说法正确的是( )
| A. | 三种元素形成的离子半径与原子半径大小顺序相同 | |
| B. | Z是地壳中含量最多的元素 | |
| C. | M、N、R晶体类型相同 | |
| D. | 少量M、N投入水中所得溶液的溶质相同 |
6.下列实验操作过程和结论都正确的是( )
0 152814 152822 152828 152832 152838 152840 152844 152850 152852 152858 152864 152868 152870 152874 152880 152882 152888 152892 152894 152898 152900 152904 152906 152908 152909 152910 152912 152913 152914 152916 152918 152922 152924 152928 152930 152934 152940 152942 152948 152952 152954 152958 152964 152970 152972 152978 152982 152984 152990 152994 153000 153008 203614
| A. | 用浓硫酸吸收二氧化硫中混有少量SO3气体 | |
| B. | 除去NaCl晶体中少量KNO3,可以将混合物制成热的饱和溶液,然后冷却结晶,过滤 | |
| C. | HClO溶液有漂白性,无法用pH试纸或pH计测得0.1mol/L的HClO溶液的pH值 | |
| D. | 在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、普通玻璃棒进行搅拌使酸和碱充分反应、准确读取实验时温度计最高温度、并且取2~3次的实验平均值等措施,已达到良好的实验结果 |

 .
. 、
、 ,属于两性化合物的电离方程式Al3++3OH-?Al(OH)3 ?H++AlO2-+H2O.
,属于两性化合物的电离方程式Al3++3OH-?Al(OH)3 ?H++AlO2-+H2O.