19.室温下,强酸性和强碱性溶液中都不能共存的离子组是( )
| A. | NH4+、Cu2+、SO42-、NO3- | B. | Mg2+、Fe2+、NO3-、I- | ||
| C. | K+、Na+、Al3+、SO42- | D. | K+、Na+、SO32-、S2- |
18. 硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等.有关物质的部分性质如表:
硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等.有关物质的部分性质如表:
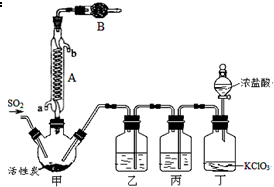
实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,装置如图所示(夹持仪器已省略),请回答有关问题:
(1)仪器A冷却水的进口为a(填“a”或“b”).
(2)仪器B中盛放的药品是碱石灰.
(3)实验时,装置丁中发生反应的离子方程式为ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(4)装置丙的作用为除去Cl2中的HCl,若缺少装置乙,则硫酰氯会水解,该反应的化学方程式为SO2Cl2+2H2O═H2SO4+2HCl.
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H═H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸.
①从分解产物中分离出硫酰氯的方法是蒸馏.
②请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):取产物在干燥条件下加热至完全反应(或挥发或分解等),冷却后加水稀释;取少量溶液滴加紫色石蕊试液变红;再取少量溶液,加入BaCl2溶液产生白色沉淀,说明含有H2SO4.或取反应后的产物直接加BCl2溶液,有白色沉淀,再滴加紫色石蕊试液变红,说明含有H2SO4.
 硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等.有关物质的部分性质如表:
硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等.有关物质的部分性质如表:| 物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 ②易分解:SO2Cl2$\frac{\underline{\;100℃\;}}{\;}$SO2↑+Cl2↑ |
| H2SO4 | 10.4 | 338 | 吸水性且不易分解 |
(1)仪器A冷却水的进口为a(填“a”或“b”).
(2)仪器B中盛放的药品是碱石灰.
(3)实验时,装置丁中发生反应的离子方程式为ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(4)装置丙的作用为除去Cl2中的HCl,若缺少装置乙,则硫酰氯会水解,该反应的化学方程式为SO2Cl2+2H2O═H2SO4+2HCl.
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H═H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸.
①从分解产物中分离出硫酰氯的方法是蒸馏.
②请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):取产物在干燥条件下加热至完全反应(或挥发或分解等),冷却后加水稀释;取少量溶液滴加紫色石蕊试液变红;再取少量溶液,加入BaCl2溶液产生白色沉淀,说明含有H2SO4.或取反应后的产物直接加BCl2溶液,有白色沉淀,再滴加紫色石蕊试液变红,说明含有H2SO4.
15.镁及铁是用途很广的金属材料,某学校研究性学习小组从工业废水(主要含Mg2+、Fe3+、Cl-)中模拟工业生产来提取镁和铁,主要过程如下:回答下列问题

(1)试剂①可以是AB
A.MgCO3 B.Mg(OH)2C.NaOH D.NH3•H2O
其目的是使溶液的pH升高,使Fe3+转化为氢氧化铁沉淀而分离出去.
(2)图1是该校研究性学习小组设计进行过程③的实验装置图.其中装置A的作用是制备干燥的HCl气体,抑制MgCl2的水解.
(3)为了分析废水中铁元素的含量,先将废水预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂?否(填“是”或“否”),请说明理由KMnO4溶液自身可作指示剂.
②下列滴定操作可使测量结果偏大的是ACD.
A.锥形瓶水洗后.用待测液润洗过再装待测液.
B.滴定前读数仰视.滴定后读数俯视.
C.滴定管水洗后.未用标准液洗涤.
D.滴定管装液后尖嘴部位有气泡,滴定后气泡消失
③某同学称取5.000g废水,预处理后在容量瓶中配制成100ml溶液,移取25.00ml试样溶液,用1.000×10-2mol•L-1KMnO4标准溶液滴定.三次实验的实验数据如下表所示.,则废水中铁元素的质量分数是4.480%.
0 152709 152717 152723 152727 152733 152735 152739 152745 152747 152753 152759 152763 152765 152769 152775 152777 152783 152787 152789 152793 152795 152799 152801 152803 152804 152805 152807 152808 152809 152811 152813 152817 152819 152823 152825 152829 152835 152837 152843 152847 152849 152853 152859 152865 152867 152873 152877 152879 152885 152889 152895 152903 203614
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Fe3+ | 2.7 | 3.7 |

(1)试剂①可以是AB
A.MgCO3 B.Mg(OH)2C.NaOH D.NH3•H2O
其目的是使溶液的pH升高,使Fe3+转化为氢氧化铁沉淀而分离出去.
(2)图1是该校研究性学习小组设计进行过程③的实验装置图.其中装置A的作用是制备干燥的HCl气体,抑制MgCl2的水解.
(3)为了分析废水中铁元素的含量,先将废水预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂?否(填“是”或“否”),请说明理由KMnO4溶液自身可作指示剂.
②下列滴定操作可使测量结果偏大的是ACD.
A.锥形瓶水洗后.用待测液润洗过再装待测液.
B.滴定前读数仰视.滴定后读数俯视.
C.滴定管水洗后.未用标准液洗涤.
D.滴定管装液后尖嘴部位有气泡,滴定后气泡消失
③某同学称取5.000g废水,预处理后在容量瓶中配制成100ml溶液,移取25.00ml试样溶液,用1.000×10-2mol•L-1KMnO4标准溶液滴定.三次实验的实验数据如下表所示.,则废水中铁元素的质量分数是4.480%.
| 实验 编号 | 待测溶液的体积(mL) | 滴定前标液的 体积读数(mL) | 滴定后标液的 体积读数(mL) |
| 1 | 20.00 | 1.20 | 21.22 |
| 2 | 20.00 | 2.21 | 22.19 |
| 3 | 20.00 | 1.50 | 23.48 |
 某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:SO2>I->Fe2+,用如图所示装置进行实验(加热和夹持装置已略,气密性已检验).
某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:SO2>I->Fe2+,用如图所示装置进行实验(加热和夹持装置已略,气密性已检验).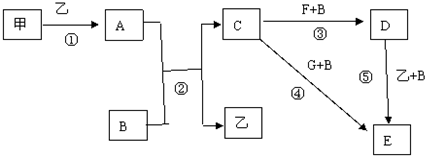
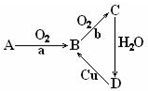

 某学习小组欲制取氨气并探究其性质.请回答:
某学习小组欲制取氨气并探究其性质.请回答: