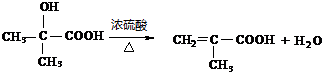4.一定温度下可逆反应:A(s)+2B(g)?2C(g)+D(g);△H>0.现将1molA和2molB加入 甲容器中,将4molC和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动).下列说法正确的是( )


| A. | 保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
18. 25℃时,已知H2CO3?H++HCO3-K1=4.3×l0-7;
25℃时,已知H2CO3?H++HCO3-K1=4.3×l0-7;
HCO3-?H++CO32-K2=5.6×l0-11;
H2O?H++OH-Kw=1.0×l0-14
现取10.6g Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
 25℃时,已知H2CO3?H++HCO3-K1=4.3×l0-7;
25℃时,已知H2CO3?H++HCO3-K1=4.3×l0-7;HCO3-?H++CO32-K2=5.6×l0-11;
H2O?H++OH-Kw=1.0×l0-14
现取10.6g Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
| A. | W点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-) | |
| B. | pH=4的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1 mol•L-1 | |
| C. | pH=8的溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-) | |
| D. | pH=11的溶液中:CO32-+H2O?HCO3-+OH-K=1.8×l0-4 |
17. 工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置如图所示.下列说法正确的是( )
工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置如图所示.下列说法正确的是( )
 工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置如图所示.下列说法正确的是( )
工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置如图所示.下列说法正确的是( )| A. | 为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环的物质A为CO2 | |
| B. | 甲装置中阴极的反应为Fe-2e-═Fe2+ | |
| C. | 为了增加污水的导电能力,应向污水中如入适量的NaOH溶液 | |
| D. | 当乙装置中有1.6 g CH4参加反应,则C电极理论上生成气体在标准状况下为4.48 L |
16.下列关于有机物的说法正确的是( )
0 152425 152433 152439 152443 152449 152451 152455 152461 152463 152469 152475 152479 152481 152485 152491 152493 152499 152503 152505 152509 152511 152515 152517 152519 152520 152521 152523 152524 152525 152527 152529 152533 152535 152539 152541 152545 152551 152553 152559 152563 152565 152569 152575 152581 152583 152589 152593 152595 152601 152605 152611 152619 203614
| A. | 按系统命名法,化合物 的名称为:2,3,3,8,8-五甲基壬烷 的名称为:2,3,3,8,8-五甲基壬烷 | |
| B. | 将少量溴水加入石油裂化得到的汽油中,溴水分层,上层为橙红色 | |
| C. | 往2ml10%的CuSO4溶液中加入5滴5%的NaOH溶液,再加入2ml10%的葡萄糖溶液,加热,得到砖红色的氧化亚铜沉淀 | |
| D. | 甲烷、乙醇、乙酸在一定条件下都能发生取代反应 |
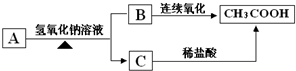

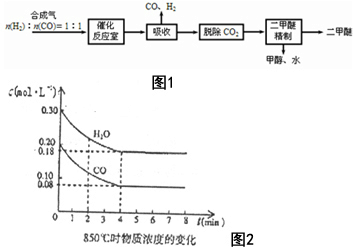 二甲醚(CH3OCH3)是一种清洁、高效、具有优良的环保性能的可燃物,被称为21世纪的新型能源.工业制备二甲醚的生产流程如图1:
二甲醚(CH3OCH3)是一种清洁、高效、具有优良的环保性能的可燃物,被称为21世纪的新型能源.工业制备二甲醚的生产流程如图1:
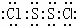 ,二氯化二硫(S2Cl2)所属的晶体类型分子晶体.
,二氯化二硫(S2Cl2)所属的晶体类型分子晶体.

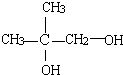 .
.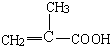 .
.