20.海水资源的综合利用十分重要,不需要通过化学变化就能够从海水中获得的物质是( )
| A. | 食盐、淡水 | B. | 钠、镁 | C. | 烧碱、氯气 | D. | 溴、碘 |
18.化学与生产、生活密切相关,下列有关说法不正确的是( )
| A. | 同位素的应用已经遍及医学、工业、农业、能源和科学研究的各个领域 | |
| B. | iPhone5外壳易掉色,是因为铝壳表面氧化处理过程中作为阴极的金属铝纯度不够,导致氧化膜不够致密 | |
| C. | 利用太阳能、风能和氢能等能源替代化石能源有利于实现“低碳经济” | |
| D. | 在医疗上硫酸亚铁可用于生产防治缺铁性贫血的药剂,在工业上硫酸亚铁还是生产铁系列净水剂的原料 |
16.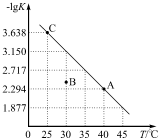 将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )
将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )
 将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )
将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )| A. | 该反应的△H>0 | |
| B. | 30℃时,B点对应状态的v(正)<v(逆) | |
| C. | A点对应状态的平衡常数K(A)=10-2.294 | |
| D. | NH3的体积分数不变时,该反应一定达到平衡状态 |
15.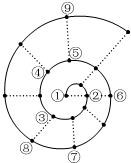 如果将前18号元素按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列有关说法正确的是( )
如果将前18号元素按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列有关说法正确的是( )
 如果将前18号元素按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列有关说法正确的是( )
如果将前18号元素按原子序数递增的顺序排列,可形成图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列有关说法正确的是( )| A. | 最简单气态氢化物的稳定性:③比⑧强、⑤比⑨弱 | |
| B. | 最高价氧化物对应水化物的碱性:②比⑥强 | |
| C. | ⑦的最高价氧化物对应的水化物具有两性 | |
| D. | 简单离子半径④比⑥小 |
14.NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,22.4 LBr2所含溴原子的数目为2NA | |
| B. | 常温下,NO2与足量的水反应生成0.1molNO,转移的电子数为0.2NA | |
| C. | 1 mol 乙醇中含有的C-H键的数目为6NA | |
| D. | 1mol•L-1的NaClO溶液中含有的ClO-数目小于NA |
13.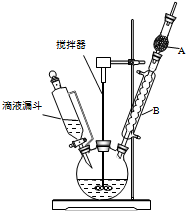 三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.
三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.
已知:①过程中生成的中间物质格氏试剂易发生水解反应;
②部分相关物质的沸点如下:
③三苯甲醇的相对分子质量为260.
请回答下列问题:
(1)装置中玻璃仪器B的名称为冷凝管;装有无水CaCl2的仪器A的作用是防止空气中的水蒸气进入装置,避免格氏试剂水解.
(2)装置中滴加液体未用普通分液漏斗而用滴液漏斗的作用是平衡压强,使漏斗内液体顺利滴下;制取格氏试剂时要保持温度约为40℃,可以采用水浴加热方式.
(3)制得的三苯甲醇粗产品中含有乙醚、溴苯、氯化铵等杂质,可以设计如下提纯方案:
粗产品$\stackrel{①操作}{→}$$\stackrel{②溶解、过滤}{→}$$\stackrel{③洗涤、干燥}{→}$三苯甲醇,其中,操作①的名称是蒸馏或分馏;洗涤液最好选用a(填字母序号).
a.水 b.乙醚 c.乙醇 d.苯
检验产品已经洗涤干净的操作为取少量最后一次洗涤液于试管中,滴加硝酸银溶液,若无沉淀生成,则已洗涤干净,反之则未洗涤干净.
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不反应),充分反应后,测得生成的气体在标准状况下的体积为100.80mL.则产品中三苯甲醇的质量分数为90%.
 三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.
三苯甲醇(C6H5)3C-OH是一种重要的化工原料和医药中间体.实验室合成三苯甲醇的实验装置如图所示.已知:①过程中生成的中间物质格氏试剂易发生水解反应;
②部分相关物质的沸点如下:
| 物质 | 沸点/℃ |
| 三苯甲醇[ | 380 |
| 乙醚 | 34.6 |
| 溴苯 | 156.2 |
请回答下列问题:
(1)装置中玻璃仪器B的名称为冷凝管;装有无水CaCl2的仪器A的作用是防止空气中的水蒸气进入装置,避免格氏试剂水解.
(2)装置中滴加液体未用普通分液漏斗而用滴液漏斗的作用是平衡压强,使漏斗内液体顺利滴下;制取格氏试剂时要保持温度约为40℃,可以采用水浴加热方式.
(3)制得的三苯甲醇粗产品中含有乙醚、溴苯、氯化铵等杂质,可以设计如下提纯方案:
粗产品$\stackrel{①操作}{→}$$\stackrel{②溶解、过滤}{→}$$\stackrel{③洗涤、干燥}{→}$三苯甲醇,其中,操作①的名称是蒸馏或分馏;洗涤液最好选用a(填字母序号).
a.水 b.乙醚 c.乙醇 d.苯
检验产品已经洗涤干净的操作为取少量最后一次洗涤液于试管中,滴加硝酸银溶液,若无沉淀生成,则已洗涤干净,反之则未洗涤干净.
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不反应),充分反应后,测得生成的气体在标准状况下的体积为100.80mL.则产品中三苯甲醇的质量分数为90%.
12.做实验时不小心使皮肤上沾了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(乙二酸)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为:MnO4-+H2C2O4+H+═CO2↑+Mn2++□下列有关叙述不正确的是(?)
| A. | 该反应的氧化剂为KMnO4 | |
| B. | 发生还原反应的是H2C2O4 | |
| C. | 该离子方程式右侧方框内的产物是H2O | |
| D. | 6mol H+参加反应时,电子转移10mol |
11.茉莉醛具有浓郁的茉莉花香,其结构简式如下所示: 关于茉莉醛的下列叙述不正确的是 (?)
关于茉莉醛的下列叙述不正确的是 (?)
0 152311 152319 152325 152329 152335 152337 152341 152347 152349 152355 152361 152365 152367 152371 152377 152379 152385 152389 152391 152395 152397 152401 152403 152405 152406 152407 152409 152410 152411 152413 152415 152419 152421 152425 152427 152431 152437 152439 152445 152449 152451 152455 152461 152467 152469 152475 152479 152481 152487 152491 152497 152505 203614
 关于茉莉醛的下列叙述不正确的是 (?)
关于茉莉醛的下列叙述不正确的是 (?)| A. | 茉莉醛能使溴水褪色 | |
| B. | 在加热和催化剂作用下,能被氢气还原生成一种芳香醇 | |
| C. | 一定条件下,能被银氨溶液、新制氢氧化铜等多种氧化剂氧化 | |
| D. | 不能与氢溴酸发生加成反应 |
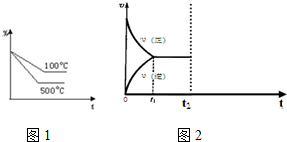
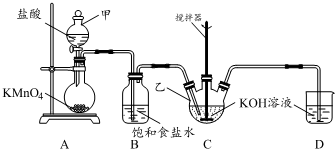 实验室用图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4.
实验室用图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4.