��Ŀ����
17��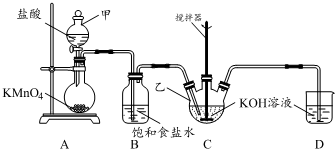 ʵ������ͼ��ʾװ���Ʊ�KClO��Һ����ͨ��KClO��Һ��Fe��NO3��3��Һ�ķ�Ӧ�Ʊ���Чˮ������K2FeO4��
ʵ������ͼ��ʾװ���Ʊ�KClO��Һ����ͨ��KClO��Һ��Fe��NO3��3��Һ�ķ�Ӧ�Ʊ���Чˮ������K2FeO4����֪K2FeO4�����������ʣ�
�ٿ�����ˮ������ŨKOH��Һ
����0�桫5�桢ǿ������Һ�бȽ��ȶ�
����Fe3+��Fe��OH��3�������·����ֽ�
���������������������£�����ˮ��Ӧ����Fe��OH��3��O2
��1��д���������ҵ����ƣ���Һ©������������ƿ��
��2��װ��C�з�����Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O��װ��D�����������ն����������
��3��Cl2��KOH�ڽϸ��¶��·�Ӧ����KClO3���ڲ��ı�KOH��Һ��Ũ�Ⱥ�����������£������Ʒ�Ӧ��0�桫5����У�ʵ���пɲ�ȡ�Ĵ�ʩ�ǣ������μ����ᡢװ��C�ñ�ˮԡ�У�
��4��д��K2FeO4����������������ˮ��Ӧ����Fe��OH��3��O2�Ļ�ѧ����ʽ��4K2FeO4+10H2O=8KOH+4Fe��OH��3��+3O2����
��5����ҵ�ϳ��á���ӵ��������ⶨ���������Ʒ�и�����صĺ������䷽���ǣ��ü��Եĵ⻯����Һ��pHΪ11��12���ܽ�3.96g���������Ʒ������pHΪ1���ܹ����40��������Ӧ��ȫ�������������ȫ������ԭ�������ӣ����ٵ���pHΪ3��4�������ԣ�����1.0mol/L����������Ʊ���Һ��Ϊ�ζ������еζ���2Na2S2O3+I2�TNa2S4O6+2NaI�������ﵽ�ζ��յ�ʱ����ȥ��������Ʊ���Һ15.00mL����ԭ���������Ʒ�и�����ص���������Ϊ25%��
���� ����ʵ��װ��ͼ��֪��Aװ�� ���ø�����������ᷴӦ�Ƶ��������������лӷ����������Ȼ��⣬����Bװ���б���ʳ��ˮ�dz�ȥ�����е��Ȼ��⣬װ��C��������������������ҺӦ�Ƶô������ƣ���Ӧ��β�������������������գ�
��1������װ��ͼ��֪�������ƣ�
��2���������������ط�Ӧ�����Ȼ��غʹ�����أ������ж�����Ҫ����β�����գ�
��3��Cl2��KOH�ڽϸ��¶��·�Ӧ����KClO3����ȡKClO�¶ȷ�Ӧ��0�桫5�棬װ��CӦ���ڱ�ˮԡ�У�Ӧ����ͨ�����������ʣ�
��4������Ԫ���غ�͵��ӵ�ʧ�غ��д��K2FeO4����������������ˮ��Ӧ����Fe��OH��3��O2�Ļ�ѧ����ʽ��
��5���ü��Եĵ⻯����Һ�ܽ���������Ʒ������pHΪ1���������������ӷ���������ԭ��Ӧ�������������ȫ������ԭ�������ӣ������ӱ������ɵ⣬���ݵ��ӵ�ʧ�غ��й�ϵ2FeO42-��3I2���ٸ��ݷ�Ӧ2Na2S2O3+I2�TNa2S4O6+2NaI��������������Ƶ����ʵ����ɼ���ø�����ص�����������ȷ������������
��� �⣺��1������װ��ͼ��֪�����������Ƿ�Һ©���������ҵ�������������ƿ��
�ʴ�Ϊ����Һ©����������ƿ��
��2���������������ط�Ӧ�����Ȼ��غʹ�����أ���Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O�������ж�����Ҫ����β�����գ�����װ��D�����������ն����������
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O�����ն����������
��3��Cl2��KOH�ڽϸ��¶��·�Ӧ����KClO3����ȡKClO�¶ȷ�Ӧ��0�桫5�棬װ��CӦ���ڱ�ˮԡ�У������μ����ᣬ�����������������ʣ�
�ʴ�Ϊ�������μ����ᡢװ��C�ñ�ˮԡ�У�
��4��K2FeO4����������������ˮ��Ӧ����Fe��OH��3��O2�Ļ�ѧ����ʽΪ4K2FeO4+10H2O=8KOH+4Fe��OH��3��+3O2����
�ʴ�Ϊ��4K2FeO4+10H2O=8KOH+4Fe��OH��3��+3O2����
��5���ü��Եĵ⻯����Һ�ܽ���������Ʒ������pHΪ1���������������ӷ���������ԭ��Ӧ�������������ȫ������ԭ�������ӣ������ӱ������ɵ⣬���ݵ��ӵ�ʧ�غ��й�ϵ2FeO42-��3I2���ٸ��ݷ�Ӧ2Na2S2O3+I2�TNa2S4O6+2NaI���ù�ϵʽ2FeO42-��3I2��6Na2S2O3�����Ը�����ص�����Ϊ$\frac{1}{3}$��1.0mol/L��0.015L��198g/mol=0.99g����ԭ���������Ʒ�и�����ص���������Ϊ$\frac{0.99g}{3.96g}$��100%=25%��
�ʴ�Ϊ��25%��
���� ���⿼��ʵ���Ʊ�������������ԭ��Ӧ�ζ������㡢���ʵķ����ᴿ��������������ķ������ۣ��Ƕ�ѧ���ۺ������Ŀ��飬ע����Ŀ��Ϣ��Ǩ�����ã��Ѷ��еȣ�

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д�| A�� | �����£�14 g��ϩ�к�̼ԭ����ΪNA | |
| B�� | 1 mol NH4+��1 mol OH-�����ĵ�������Ϊ10NA | |
| C�� | ���³�ѹ�£�22.4L CH4�к�C-H����ĿΪ4NA | |
| D�� | �����£�pH=13��NaOH��Һ�к�OH-��ĿΪ0.1NA |
��H=a kJ•mol-1��
��1����֪����Fe2O3��s��+3C��s��ʯī��=2Fe��s��+3CO��g��
��H1=+489.0kJ•mol-1��
��C��s��ʯī��+CO2��g��=2CO��g����H2=+172.5kJ•mol-1����a=-28.5��
��2��ұ������Ӧ��ƽ�ⳣ������ʽK=$\frac{{c}^{3}��C{O}_{2}��}{{c}^{3}��CO��}$���¶����ߺ�Kֵ��С������������䡱��С������
��3����T��ʱ���÷�Ӧ��ƽ�ⳣ��K=64����2L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⣮
| Fe2O3 | CO | Fe | CO2 | |
| ��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| ��/mol | 1.0 | 2.0 | 1.0 | 1.0 |
������˵����ȷ����ad������ĸ����
a���������������ܶȺ㶨ʱ����־��Ӧ�ﵽƽ��״̬
b������Fe2O3�������������CO��ת����
c����������CO��ƽ��ת���ʴ����ҵ�ƽ��ת����
d���ס��������У�CO��ƽ��Ũ��֮��Ϊ2��3
��4����ȡһ����ʩ�ɷ�ֹ������ʴ������װ���е��ձ����ʢ�е�Ũ�ȡ��������NaCl��Һ��
����a��b��cװ�����ܱ���������bc������ĸ����
������dװ�ñ�������X���ĵ缫����Ӧ��п�������ƣ���

��5��25��ʱ�й����ʵ��ܶȻ����£�Ksp[Mg��OH��2]=5.61��10-12��Ksp[Fe��OH��3]=2.64��10-39��25��ʱ������Mg2+��Fe3+����Һ�еμ�NaOH��Һ�������ֳ�����������Һ��pH=8ʱ��c��Mg2+����c��Fe3+��=2.215��1021��
| A�� | �÷�Ӧ��������ΪKMnO4 | |
| B�� | ������ԭ��Ӧ����H2C2O4 | |
| C�� | �����ӷ���ʽ�Ҳ���ڵIJ�����H2O | |
| D�� | 6mol H+�μӷ�Ӧʱ������ת��10mol |
 ��ͼ�Թ���ʢ��������ݹ���������U�ι���ʢ��һ�κ�īˮ����ʼʱU����˺�īˮˮ���½���һ��ʱ���U����˺�īˮˮ��������������˵������ȷ���ǣ�������
��ͼ�Թ���ʢ��������ݹ���������U�ι���ʢ��һ�κ�īˮ����ʼʱU����˺�īˮˮ���½���һ��ʱ���U����˺�īˮˮ��������������˵������ȷ���ǣ�������| A�� | ��ʼʱ�����������ⸯʴ | B�� | -��ʱ���������������ʴ | ||
| C�� | ����ʱ���ڸ����ĵ缫��Ӧ��ͬ | D�� | ����ʱ���������ĵ缫��Ӧ��ͬ |
| A�� | ����������Ӧ | B�� | ���Դ�������� | C�� | �Dz��缫 | D�� | �õ��� |
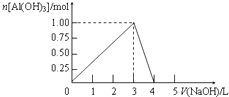 �����Ϊ0.5L��AlCl3��Һ������ijŨ�ȵ�NaOH��Һ���õ��ij�����NaOH��Һ����ı仯��ͼ��ʾ�����н����ȷ���ǣ�������
�����Ϊ0.5L��AlCl3��Һ������ijŨ�ȵ�NaOH��Һ���õ��ij�����NaOH��Һ����ı仯��ͼ��ʾ�����н����ȷ���ǣ�������| A�� | ��Ӧ�����У��������ʱ������Ϊ7.8g | |
| B�� | AlCl3��Һ��Ũ��Ϊ2.0��mol•L-1 | |
| C�� | �õ�39g����ʱ�����ĵ�NaOH��Һ���Ϊ1.5L��3.5L | |
| D�� | ��V��NaOH��=4Lʱ���õ�����Һ��Na+��Cl-Ũ����� |
| A�� | Y���ʲ�����X���⻯�ﷴӦ | |
| B�� | Y���⻯�������ӻ����� | |
| C�� | ��ҵ��ұ��Zͨ���õ���������Ȼ���ķ��� | |
| D�� | W���ʼ������ᷴӦ��������Ӧ�������������� |
 �������ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫��
�������ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫��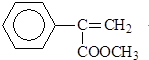 ��
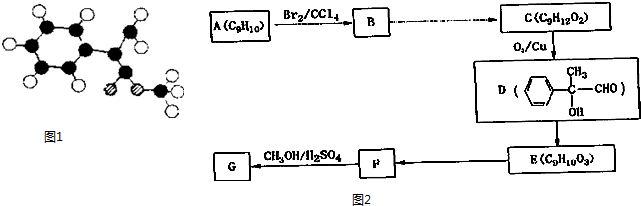
��
 ��
�� ��
��