16.铜的冶炼大致可分为:
(1)富集,将硫化物矿进行浮选;
(2)焙烧,主要反应为2Cu+FeS2+4O2═Cu2S+3SO2+2FeO(炉渣);
(3)制粗铜,在1200℃发生的主要反应为:2Cu2S+3O2═2Cu2O+2SO2,2Cu2O+Cu2S═6Cu+SO2;
(4)电解精炼.
下列说法正确的是( )
(1)富集,将硫化物矿进行浮选;
(2)焙烧,主要反应为2Cu+FeS2+4O2═Cu2S+3SO2+2FeO(炉渣);
(3)制粗铜,在1200℃发生的主要反应为:2Cu2S+3O2═2Cu2O+2SO2,2Cu2O+Cu2S═6Cu+SO2;
(4)电解精炼.
下列说法正确的是( )
| A. | 上述灼烧过程的尾气均可直接排到空气中 | |
| B. | 由6 mol CuFeS2生成6 mol Cu,上述共消耗15 mol O2 | |
| C. | 在反应2Cu2O+Cu2S═6Cu+SO2中,作氧化剂的只有Cu2O | |
| D. | 电解精炼时,粗铜应与外电源正极相连 |
15.下列离子检验的推理正确的是( )
| A. | 向某溶液中加盐酸,有能使澄清石灰水变浑浊的气体生成,则原溶液中有CO32- | |
| B. | 向某溶液中加石蕊试液,溶液变红,则原溶液中溶质是酸 | |
| C. | 向某溶液中加氢氧化钠溶液,生成蓝色沉淀,则原溶液中有Cu2+ | |
| D. | 向某溶液中加氯化钡溶液,生成白色沉淀,再加盐酸沉淀不溶解,则原溶液中有SO42- |
14.下列反应的离子方程式正确的是( )
| A. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| B. | 向三氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═A1(OH)3↓+3NH4+ | |
| C. | 向碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 石灰石溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O |
11.将5.6g Cu、Mg合金投入到一定量的硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下混合气体VL(HNO3被还原为NO和NO2);若向反应后的溶液中加入足量氢氧化钠溶液,待金属元素全部沉淀后,再将沉淀过滤、洗净、干燥后称量质量为10.7g,则下列分析正确的是( )
| A. | 沉淀中氢氧根的质量为5.1g | B. | V为2.24L | ||
| C. | Cu的物质的量为0.1mol | D. | 反应后溶液呈中性 |
10.下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 某弱酸的酸式盐NaHA溶液中一定有:c(OH-)+2c(A2-)═c(H+)+c(H2A) | |
| B. | 0.1 mol•L-1CH3COONa 溶液与0.05 mol•L-1盐酸等体积混合后的酸性溶 液中:c(CH3COO-)>c(CH3COOH)>c(Cl-)=c(H+) | |
| C. | 物质的量浓度相等的HCN溶液和NaCN溶液等体积混合后的溶液中:c(CN-)+c(OH-)═c(H+)+c(Na+) | |
| D. | 0.1 mol•L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3•H2O)+c(Fe2+)=0.3 mol•L-1 |
9.下列现象不适宜用勒夏特列原理解释的是( )
0 152260 152268 152274 152278 152284 152286 152290 152296 152298 152304 152310 152314 152316 152320 152326 152328 152334 152338 152340 152344 152346 152350 152352 152354 152355 152356 152358 152359 152360 152362 152364 152368 152370 152374 152376 152380 152386 152388 152394 152398 152400 152404 152410 152416 152418 152424 152428 152430 152436 152440 152446 152454 203614
| A. | 实验室用排饱和食盐水来收集氯气 | B. | 夏天的食物更易腐蚀 | ||
| C. | 氨水适宜保存在低温处 | D. | 醋酸能用来清洗水垢 |
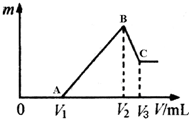 将0.1mol的镁、铝混合物溶于100mL 4mol/LHCl溶液中,然后再滴加1mol/L NaOH溶液.请回答:
将0.1mol的镁、铝混合物溶于100mL 4mol/LHCl溶液中,然后再滴加1mol/L NaOH溶液.请回答: