13. 车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如下表:
车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如下表:
(1)写出NO与活性炭反应的化学方程式C+2NO?N2+CO2.
(2)上述反应T1℃时的平衡常数K1=4.
(3)上述反应T1℃时达到平衡后,再通入0.1mol的NO的气体,则达到新平衡时NO的转化率为80%.
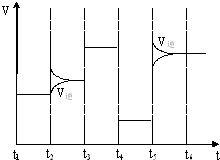
(4)如图为在T1℃达到平衡后在t2、t3、t4、t5时改变某一种反应条件,平衡体系中速率随时间变化的情况,
且所改变的条件均不同.已知t3-t4阶段为使用催化剂.请判断温度的高低T1<T2,该反应△H<0.
 车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如下表:
车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如下表:| 物质 T/℃ | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
(2)上述反应T1℃时的平衡常数K1=4.
(3)上述反应T1℃时达到平衡后,再通入0.1mol的NO的气体,则达到新平衡时NO的转化率为80%.
(4)如图为在T1℃达到平衡后在t2、t3、t4、t5时改变某一种反应条件,平衡体系中速率随时间变化的情况,
且所改变的条件均不同.已知t3-t4阶段为使用催化剂.请判断温度的高低T1<T2,该反应△H<0.
12.25℃时,向10.0mL 0.2mol•L-1CH3COOH溶液中逐滴滴入0.1mol•L-1的NaOH溶液,下列有关溶液中微粒的物质的量浓度关系不正确的是( )
| A. | 过程中可能有:c(Na+)>c(OH-)=c(CH3COO-)>c(H+) | |
| B. | 整个过程中都有:c(OH-)-c(H+)=c(Na+)-c(CH3COO-) | |
| C. | 当滴入10.0 mLNaOH溶液时有:c(CH3COOH)-c(CH3COO-)═2[c(OH-)-c(H+)] | |
| D. | 当滴入10.0 mLNaOH溶液时混合溶液的pH=4.75,则:c(CH3COO-)>c(CH3COOH)>c(Na+)>c(H+)>c(OH-) |
11.下列关于乙酸的说法不正确的是( )
| A. | 可以除去热水瓶内胆水垢 | B. | 具有挥发性 | ||
| C. | 能与乙醇反应生成有香味的酯 | D. | 能发生加聚反应 |
10.干冰不能用来扑灭镁条火灾,反应为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,该反应属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
9.下列过程放出热量的是( )
| A. | 氢气在氯气中燃烧 | B. | 液氨气化 | ||
| C. | 碳酸钙分解 | D. | H-Cl→H+Cl |
8.“84”消毒液的有效成分是( )
| A. | NaClO | B. | NaCl | C. | NaOH | D. | Na2CO3 |
7.下列物质中属于碱的是( )
0 152236 152244 152250 152254 152260 152262 152266 152272 152274 152280 152286 152290 152292 152296 152302 152304 152310 152314 152316 152320 152322 152326 152328 152330 152331 152332 152334 152335 152336 152338 152340 152344 152346 152350 152352 152356 152362 152364 152370 152374 152376 152380 152386 152392 152394 152400 152404 152406 152412 152416 152422 152430 203614
| A. | KNO3 | B. | O3 | C. | Ca(OH)2 | D. | HNO3 |