11.根据相应的图象,判断下列相关说法正确的是( )


| A. | 密闭容器中反应达到平衡,t0时改变某一条件有如图变化所示,则改变的条件只能是加入催化剂 | |
| B. | 反应达到平衡时外界条件对平衡影响关系如图B所示,则正反应为放热反应,且a>b | |
| C. | 物质的量和温度关系如图C所示,则该反应的正反应为放热反应 | |
| D. | 反应速率和反应条件变化关系如图D所示,则该反应的正反应为放热反应,且A、B、C、D均为气体 |
10.在一定温度下体积固定的密闭容器中,当下列物理量:①混合气体的压强②混合气体的平均摩尔质量③混合气体的密度④A的物质的量浓度:均不再变化时,能表明可逆反应A(s)+2B(g)?C(g)+D(g)已达平衡的是( )
| A. | ①② | B. | ②③ | C. | ①④ | D. | 只有④ |
9.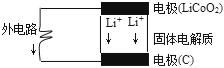 锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
 锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )| A. | 该电池的负极为LiCoO2 | |
| B. | 电池中的固体电解质可以是熔融的氯化钠、干冰等 | |
| C. | 充电时的阴极反应:Li1-xCoO2+xLi++xe-═LiCoO2 | |
| D. | 外电路上的“→”表示放电时的电子流向 |
8.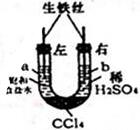 利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
 利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )
利用如图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间.下列说法不正确的是( )| A. | a管发生吸氧腐蚀,b管发生析氢腐蚀 | |
| B. | 一段时间后,a管液面高于b管液面 | |
| C. | a处、b处溶液的pH都增大 | |
| D. | a、b两处具有相同的电极反应式:Fe-3e-═Fe3+ |
7.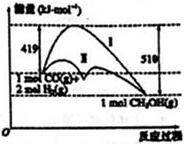 已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )
已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )
 已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )
已知某反应过程在不同条件下的能量变化情况如图所示(改变的条件仅为催化剂),下列判断错误的是( )| A. | 反应物的总能量大于生成物的总能量 | |
| B. | 曲线Ⅰ和曲线Ⅱ相比较,曲线Ⅱ使用了催化剂 | |
| C. | 该反应可以表示为:CO(g)+2H2(g)?CH3OH(g)△=0.91KJ•mol-1 | |
| D. | 如果该反应生成液态CH3OH,则△H增大 |
6.反应A(g)+B(g)?2C(g);△H<0,达到平衡时,下列说法正确的是( )
| A. | 其他条件不变,减小容器体积,平衡不移动 | |
| B. | 其他条件不变,增大c(A),A的转化率增大 | |
| C. | 降低温度,v正增大,v逆减小 | |
| D. | v正(A)═2v逆(C) |
5.已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=akJ•mol-1,平衡常数为K测得在不同温度下,K值如下:
(1)写成该反应的平衡常数表达式$\frac{[CO]}{[C{O}_{2}]}$.
(2)该反应为吸热(选填“吸热”或“放热”)反应.
(3)700℃时反应达到平衡状态,要使该平衡向右移动,其他条件不变时,可以采取的措施有BC(填序号).
A.缩小反应器体积 B.通入CO2C.升高温度到900℃D.使用合适的催化剂 E.增加Fe的量
(4)下列图象符合该反应的是A(填序号)(图中v为速率,φ为混合物中CO含量,T为温度且T1>T2).

0 152170 152178 152184 152188 152194 152196 152200 152206 152208 152214 152220 152224 152226 152230 152236 152238 152244 152248 152250 152254 152256 152260 152262 152264 152265 152266 152268 152269 152270 152272 152274 152278 152280 152284 152286 152290 152296 152298 152304 152308 152310 152314 152320 152326 152328 152334 152338 152340 152346 152350 152356 152364 203614
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
(2)该反应为吸热(选填“吸热”或“放热”)反应.
(3)700℃时反应达到平衡状态,要使该平衡向右移动,其他条件不变时,可以采取的措施有BC(填序号).
A.缩小反应器体积 B.通入CO2C.升高温度到900℃D.使用合适的催化剂 E.增加Fe的量
(4)下列图象符合该反应的是A(填序号)(图中v为速率,φ为混合物中CO含量,T为温度且T1>T2).

 甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.