题目内容
4.在T℃时,反应2SO2(g)+O2(g)?2SO3(g)△H<0的平衡常数K=6×102(mol•L-1 )-1,某生向容积为2L的密闭容器中冲入0.4molSO2、0.18molO2和1.2molSO3的混合气体,此时该反应是否处于化学平衡状态否(填“是”或“否”),若平衡后从体系中移走SO3,则平衡向正反应方向移动(填“正反应”或“逆反应”).分析 依据向容积为2L的密闭容器中充入0.4molSO2、0.18molO2和1.2molSO3的混合气体,依据平衡常数的计算方法计算出浓度商,然后根据计算结果与化学平衡常数比较来判断是否达到平衡状态,若平衡后从体系中移走SO3,是减少生成物的浓度,根据化学平衡移动原理可知平衡正向进行.
解答 解:2L的密闭容器中充入0.4molSO2、0.18molO2和1.2molSO3的混合气体,各气体的浓度为:c(SO2)=$\frac{0.4mol}{2L}$=0.2mol/L、c(O2)=$\frac{0.18mol}{2L}$=0.09mol/L、c(SO3)=$\frac{1.2mol}{2L}$=0.6mol/L,此时的浓度商为:Qc=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})c({O}_{2})}$=$\frac{(0.6mol/L)^{2}}{(0.2mol/L)^{2}×0.09mol/L}$=100<K=600,反应正向移动,说明该反应没有达到平衡状态;若平衡后从体系中移走SO3,减少生成物的浓度,则平衡向着正反应向移动,
故答案为:否,正反应.
点评 本题考查化学平衡常数分析应用、反应进行方向判断的方法等知识,化学平衡移动原理的理解应用,平衡常数和浓度商的计算比较是解题关键,题目难度不大.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
12.下列关于SO2性质的说法正确的是( )
| A. | 无色无味 | B. | 密度比空气小 | C. | 可与Ca(OH)2反应 | D. | 可用于漂白食品 |
9.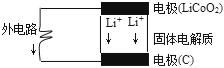 锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
 锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
锂电池的构造如图所示,电池内部“→”表示放电时Li*的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )| A. | 该电池的负极为LiCoO2 | |
| B. | 电池中的固体电解质可以是熔融的氯化钠、干冰等 | |
| C. | 充电时的阴极反应:Li1-xCoO2+xLi++xe-═LiCoO2 | |
| D. | 外电路上的“→”表示放电时的电子流向 |
16.下列关于有机物的说法中正确的是( )
①棉花、蚕丝和人造丝的主要成分都是纤维素
②淀粉、油脂、蛋白质在一定条件下都能发生水解
③易溶于汽油、酒精、苯等有机溶剂的物质都是有机化合物
④除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
⑤石油的分馏、裂化和煤的干馏都是化学变化
⑥聚碳酸酯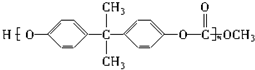 中含有
中含有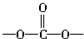 结构.
结构.
①棉花、蚕丝和人造丝的主要成分都是纤维素
②淀粉、油脂、蛋白质在一定条件下都能发生水解
③易溶于汽油、酒精、苯等有机溶剂的物质都是有机化合物
④除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液
⑤石油的分馏、裂化和煤的干馏都是化学变化
⑥聚碳酸酯
 中含有
中含有 结构.
结构.| A. | ②⑤ | B. | ②④⑥ | C. | ①②③⑥ | D. | ②④⑤ |
14.以下是一些物质的熔沸点数据(常压):
中国科学家用金属钠和CO2在一定条件下制得了金刚石:4Na+3CO2?2Na2CO3+C(s,金刚石)
完成下列填空:
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式$\frac{1}{{c}^{4}(Na)×{c}^{3}(C{O}_{2})}$.
(2)请写出一条既能提高反应速率又能提高转化率的方法:增大压强
(3)890℃,下列关于该反应的说法正确的是b(选填序号).
a.容器内气体的平均式量不再变化,则反应一定达到平衡
b.容器内固体质量不再变化,则反应一定达到平衡
c.反应起始至平衡,气体的密度不断增大
d.反应起始至平衡,容器内的压强不断增大
(4)890℃,若该反应在10L密闭容器、常压下进行,反应4h,固体质量增加56克,则二氧化碳的反应速率为0.35mol/(L•h)
(5)若温度由890℃升高到1860℃,则容器内气体的平均相对分子质量将增大(选填“增大”“减小”“不变”),
(6)若反应后要得到纯净的金刚石,请写出必要的实验操作步骤.冷却后,将反应后容器中的固体取出,加水溶解、过滤、洗涤固体并烘干,可得纯净的金刚石
(7)在此反应中,同时还会有石墨生成,已知:C(s,石墨)?C(s,金刚石)-1.9KJ,若升高温度,生成的碳单质中,金刚石的含量将增大(选填“增大”“减小”“不变”).等物质的量的石墨和金刚石中,化学键的数目较多的是金刚石.
| 钠 | Na2CO3 | 金刚石 | 石墨 | |
| 熔点(℃) | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
完成下列填空:
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式$\frac{1}{{c}^{4}(Na)×{c}^{3}(C{O}_{2})}$.
(2)请写出一条既能提高反应速率又能提高转化率的方法:增大压强
(3)890℃,下列关于该反应的说法正确的是b(选填序号).
a.容器内气体的平均式量不再变化,则反应一定达到平衡
b.容器内固体质量不再变化,则反应一定达到平衡
c.反应起始至平衡,气体的密度不断增大
d.反应起始至平衡,容器内的压强不断增大
(4)890℃,若该反应在10L密闭容器、常压下进行,反应4h,固体质量增加56克,则二氧化碳的反应速率为0.35mol/(L•h)
(5)若温度由890℃升高到1860℃,则容器内气体的平均相对分子质量将增大(选填“增大”“减小”“不变”),
(6)若反应后要得到纯净的金刚石,请写出必要的实验操作步骤.冷却后,将反应后容器中的固体取出,加水溶解、过滤、洗涤固体并烘干,可得纯净的金刚石
(7)在此反应中,同时还会有石墨生成,已知:C(s,石墨)?C(s,金刚石)-1.9KJ,若升高温度,生成的碳单质中,金刚石的含量将增大(选填“增大”“减小”“不变”).等物质的量的石墨和金刚石中,化学键的数目较多的是金刚石.
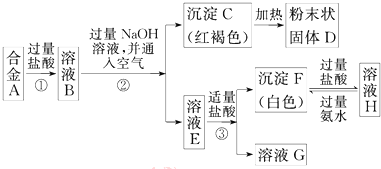
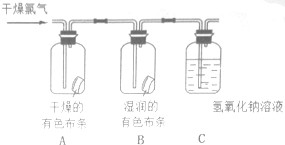 为了验证氯气的有关行政,某同学设计了如下的实验.
为了验证氯气的有关行政,某同学设计了如下的实验.