18.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1molNa2O2与SO2完全反应时转移电子数为NA | |
| B. | 18g重水(D2O)所含的电子数为10NA | |
| C. | 0.5molNH4HSO4晶体中,含有H+数目约为0.5 NA | |
| D. | 常温常压下,3gHCHO和CH3COOH的混合物中含有0.4NA个原子 |
17.将分别通入下列种溶液中,有关说法正确的是( )
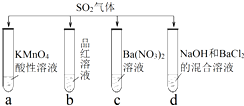

| A. | 试管a中实验可以证明具有漂白性 | |
| B. | 试管b中溶液褪色,说明具有强氧化性 | |
| C. | 试管c中能产生白色沉淀,说明具有还原性 | |
| D. | 试管d中能产生白色沉淀,该沉淀完全溶于 稀硝酸 |
15.下列中学常见实验的现象或表述正确的是( )
| A. | 检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液 | |
| B. | 过量的铁投入到一定量的稀硝酸中,充分反应后取上层清液于试管中,滴加KSCN溶液,溶液显红色 | |
| C. | 制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁 | |
| D. | 向CuSO4溶液中滴入过量NaOH溶液充分反应后,将混合液体倒入蒸发皿中加热煮沸一会,然后冷却、过滤,滤纸上的物质为“蓝色固体” |
14.对于反应2A(g)+B(g)?3C(g)+4D(g),下列数据是用不同物质的浓度变化表示的反应速率,其中反应进行得最快的是( )
| A. | v(A)=30mol•L-1•min-1 | B. | v(B)=0.3mol•L-1•s-1 | ||
| C. | v(C)=48mol•L-1•min-1 | D. | v(D)=1mol•L-1•s-1 |
13.下列离子方程式不正确的是( )
| A. | 碳酸钙与稀盐酸混合:CO32-+2H+=CO2↑+H2O | |
| B. | 硫酸铜溶液与烧碱溶液混合:Cu2++2OH-=Cu(OH)2↓ | |
| C. | 碳酸氢钠与稀盐酸混合:HCO3-+H+=CO2↑+H2O | |
| D. | 铁粉跟稀盐酸反应 2Fe+6H+=2Fe3++3H2↑ |
12.原子序数依次增大的短周期元素W、X、Y、Z,它们的最外层电子数分别为4、6、1、4.下列叙述错误的是( )
| A. | 元素的非金属性:X>W>Z | |
| B. | 元素W最高化合价和最低化合价的代数和为0 | |
| C. | Y与X能形成离子化合物 | |
| D. | 原子半径:Z>Y>X>W |
10.氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:a HClO3→b O2↑+c Cl2↑+d HClO4+e H2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色.下列说法错误的是( )
| A. | 由反应可确定:氧化性HClO3>HClO4 | |
| B. | 变蓝的淀粉碘化钾试纸褪色是因为可能发生了:4C12+I2+6H2O→12H++8Cl-+2IO3- | |
| C. | 若氯酸分解所得的混合气体的平均摩尔质量为47.6g/mol,则反应方程式可表示为:26HClO3→15O2↑+8C12↑+10HClO4+8H2O | |
| D. | 若化学计量数a=8,b=3,则该反应转移电子数为20e |
9.青蒿琥酯是治疗疟疾的首选药,可由青蒿素两步合成得到.下列有关说法正确的是 ( )
0 152016 152024 152030 152034 152040 152042 152046 152052 152054 152060 152066 152070 152072 152076 152082 152084 152090 152094 152096 152100 152102 152106 152108 152110 152111 152112 152114 152115 152116 152118 152120 152124 152126 152130 152132 152136 152142 152144 152150 152154 152156 152160 152166 152172 152174 152180 152184 152186 152192 152196 152202 152210 203614

| A. | 青蒿素分子式为C15H22O5 | |
| B. | 青蒿素不能与NaOH溶液反应 | |
| C. | 反应②原子利用率为100% | |
| D. | 青蒿琥酯能与氢氧化钠溶液反应可生成青蒿琥酯钠 |