10.25℃时,浓度均为0.1mol•L-1的HA溶液和BOH溶液,pH分别是1和11.下列说法正确的是( )
| A. | 在0.1 mol•L-1BA溶液中,c(A-)+c(H+)=c(OH-)+c(B+) | |
| B. | 若将0.1 mol•L-1 BOH溶液稀释至0.001 mol•L-1则溶液的pH=9 | |
| C. | 若将一定量的上述两溶液混合后pH=7,则混合液中:c(A-)>c(B+) | |
| D. | 若将上述两溶液按体积比1:1混合,则混合液中:c(A-)>c(B+)>c(H+)>c(OH-) |
9.某温度下,在一定体积的密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法错误的是( )
| 物质 | X | Y | Z | W |
| 初始浓度/mol•L-1 | 0.5 | 0.6 | 0 | 0 |
| 平衡浓度/mol•L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
| A. | 增大压强反应的平衡常数不变,但X的转化率增大 | |
| B. | 该反应的化学方程式为:4X (g)+5Y (g)?4Z (g)+6W (g) | |
| C. | 反应达到平衡时,X的转化率为80% | |
| D. | 其它条件不变,若增大Y的起始浓度,X的转化率增大 |
8.下列物质间反应的离子方程式正确的是( )
| A. | 相同物质的量浓度的FeI2溶液与溴水等体积混合 2Fe2++2I-+2Br2═2Fe3++I2+4Br- | |
| B. | Ba(OH)2溶液中加入过量的NaHSO4溶液 Ba2++OH-+H++SO42-═H2O+BaSO4↓ | |
| C. | 氢氧化亚铁溶液于稀硝酸中 Fe(OH)2+2H+═Fe2++2H2O | |
| D. | 向漂白粉溶液中通入少量的二氧化碳 Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO |
6.黄铁矿石的主要成分为FeS2和少量FeS(假设其他杂质中不含Fe、S元素,且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对该黄铁矿石进行如下实验探究.将m1g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全.

其反应的化学方程式为:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理:

(1)鼓入空气的作用是提供反应需要的氧气,排出装置中生成的二氧化硫被乙装置全部吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是(用化学方程式表示)Na2SO3+H2O2=Na2SO4+H2O.
H2O2可以看作是一种很弱的酸,写出其电离方程式:H2O2?H++HO2-.
(3)该黄铁矿石中硫元素的质量分数为$\frac{32m{\;}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】:测定铁元素的含量

(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
根据所给数据,计算该稀释液中Fe2+的物质的量浓度为c(Fe2+)=0.5000mol/L.
0 151942 151950 151956 151960 151966 151968 151972 151978 151980 151986 151992 151996 151998 152002 152008 152010 152016 152020 152022 152026 152028 152032 152034 152036 152037 152038 152040 152041 152042 152044 152046 152050 152052 152056 152058 152062 152068 152070 152076 152080 152082 152086 152092 152098 152100 152106 152110 152112 152118 152122 152128 152136 203614

其反应的化学方程式为:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理:

(1)鼓入空气的作用是提供反应需要的氧气,排出装置中生成的二氧化硫被乙装置全部吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是(用化学方程式表示)Na2SO3+H2O2=Na2SO4+H2O.
H2O2可以看作是一种很弱的酸,写出其电离方程式:H2O2?H++HO2-.
(3)该黄铁矿石中硫元素的质量分数为$\frac{32m{\;}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】:测定铁元素的含量

(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 20.00 | 24.97 |


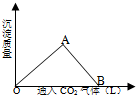 (1)在模拟溶洞的“形成”实验中,将过量二氧化碳气体通入饱和Ca(OH)2溶液中,产生CaCO3白色沉淀的质量与通入的二氧化碳气体体积之间的关系曲线如图所示.
(1)在模拟溶洞的“形成”实验中,将过量二氧化碳气体通入饱和Ca(OH)2溶液中,产生CaCO3白色沉淀的质量与通入的二氧化碳气体体积之间的关系曲线如图所示.