(1)101kPa时,1mol纯物质完全燃烧生成 时所放出的热量,叫做该物质的燃烧热,单位 ,在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ.则表示甲烷燃烧热的热化学方程式为 .
(2)在与外界隔离的体系中,自发过程将导致体系的熵 ,(填“增大”、“减小”、“不变”). 对于同一种物质, 时熵值最大.(填“固态”、“液态”、“气态”)
(3)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ•mol﹣1):
| 化学键 | C﹣H | C﹣F | H﹣F | F﹣F |
| 键能 | 414 | 489 | 565 | 158 |
根据键能数据计算以下反应的反应热△H:CH4(g)+4F2(g)=CF4(g)+4HF(g)△H= .
充满HCl的烧瓶做完喷泉实验后得到的稀盐酸,用标准碳酸钠溶液滴定这种盐酸测定它的准确浓度,请你回答下列问题:
(1)用标准Na2CO3溶液滴定这种盐酸时,Na2CO3溶液应装在 式滴定管中,若用甲基橙作指示剂,达到滴定终点时,溶液从 色变为 色.
(2)现配制三种浓度的标准Na2CO3溶液,你认为最合适的是下列第 种.
①2.500mol•L﹣1 ②0.25mol•L﹣1③0.025mol•L﹣1
(3)若采用上述合适浓度的标准Na2CO3溶液滴定,用c(Na2CO3)表示,滴定时实验数据列表如下:
| 实验次数编号 | 待 待测盐酸体积(mL) | 滴入Na2CO3 溶液体积(mL) |
| 1 | 20.00 | 19.80 |
| 2 | 20.00 | 16.95 |
| 3 | 20.00 | 17.05 |
求这种待测稀盐酸的物质的量浓度(用数据和符号列式即可):c(HCl)= .
下表是不同温度下水的离子积常数:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10﹣14 | KW | 1×10﹣12 |
试回答以下问题:
(1)若25℃<t1<t2,则KW 1×10﹣14(填“>”、“<”或“=”),判断的理由是
(2)25℃下,将pH=13的氢氧化钠溶液V1 L与pH=1的稀盐酸V2 L混合(设混合后溶液的体积为:V1+V2),所得混合溶液的pH=2,则V1:V2= .
(3)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸
性”、“中性”或“碱性”),溶液中c(Na+) c(CH3COO﹣)(填“>”、“=”或“<”).
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 性(填“酸”、“中”
或“碱”),溶液中c(Na+) c(CH3COO﹣)[填“>”、“=”或“<”]
(5)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的
pH 7(填“大于”、“小于”或“等于”);将同温度下等浓度的四种盐溶液:
A.NH4HCO3 B.NH4A C.(NH4)2SO4 D.NH4Cl
按pH由大到小的顺序排列是: (填序号).
某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针 偏转方向 |
| 1 | Mg Al | 稀盐酸 | 偏向Al |
| 2 | Al Cu | 稀盐酸 | 偏向Cu |
| 3 | Al 石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg Al | NaOH溶液 | 偏向Mg |
| 5 | Al Zn | 浓硝酸 | 偏向Al |
根据上表中的实验现象完成下列问题:
(1)实验1、2中Al所作的电极是否相同? .
(2)写出实验3中的电极反应式和电池总反应方程式.铝电极 . 石墨电极 电池总反应: .
(3)实验4中的铝作正极还是负极? ,为什么? .
(4)实验5中,负极反应为 .
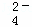 、Cl﹣、H+的物质的量浓度分别是多少?
、Cl﹣、H+的物质的量浓度分别是多少?