乌头酸的结构简式如图所示,下列关于乌头酸的说法正确的是( )

|
| A. | 化学式为C8H6O6 |
|
| B. | 乌头酸可发生加成反应和取代反应 |
|
| C. | 乌头酸分子中能发生酯化反应的官能团有2种 |
|
| D. | 1mol乌头酸与足量的钠反应生成3molH2 |
如图X、Y、A、B、C均为短周期主族元素,其中只有一种是金属元素,则下列说法错误是( )
| X | A | ||
| Y | C | B |
|
| A. | 原子半径大小:Y>C>X>A |
|
| B. | Y和B形成的化合物中Y和B的原子个数比为2:3 |
|
| C. | X、C、A中最高价氧化物对应的水化物的酸性最强的是A |
|
| D. | A、B均为非金属元素,所以两者的氢化物相遇不发生反应 |
下列与化学概念有关的说法错误的是( )
|
| A. | 水在化学反应中既可做氧化剂又可做还原剂 |
|
| B. | 14C和14N质量数相同,但化学性质不同 |
|
| C. | 牛奶是一种胶体,能发生丁达尔现象 |
|
| D. | 由同一种元素组成的物质一定是纯净物 |
氨是最重要的氮肥,是产量最大的化工产品之一。课本里介绍的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的,他因此获得了1918年诺贝尔化学奖。其合成原理为: N2(g)+3H2(g)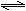 2NH3(g),其部分工艺流程如下:
2NH3(g),其部分工艺流程如下:
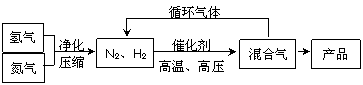

回答下列问题:
(1)已知299 K时,合成氨反应N2(g)+3H2(g)  2NH3(g) △H=-Q kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失) ▲
2NH3(g) △H=-Q kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失) ▲
A.一定大于Q kJ B.一定等于Q kJ C.一定小于Q kJ D. 不能确定
(2)已知反应:①N2(g) + O2(g) = 2NO(g) △H1=+180.5kJ/mol
②4NH3(g) + 5O2(g) = 4NO(g) + 6H2O(g) △H2=-905kJ/mol
③2H2(g) + O2(g) = 2H2O(g) △H3=-483.6kJ/mol
则N2(g)+3H2(g) 2NH3(g)的△H = ____________▲ ______________。
2NH3(g)的△H = ____________▲ ______________。
(3)可以用氯气来检验输送氨气的管道是否漏气,如果漏气则会有白烟(成份为氯化铵)生成。该反应的化学方程式为: ▲ 。
(4)一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:N2+3H2O 2NH3+
2NH3+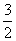 O2 进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3 h):请回答下列问题:
O2 进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3 h):请回答下列问题:
| T/℃ | 30 | 40 | 50 |
| 生成NH3量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
①50℃时从开始到3 h内以O2物质的量变化表示的平均反应速率为_____▲ mol·h-1。
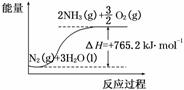
②该反应过程与能量关系可用如图表示,则反应的热化学方程式是__________________________▲________________________________________________。
③工业合成氨的热化学方程式为N2(g)+3H2(g)  2NH3(g),在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,达到平衡时,N2的转化率为50%,体积变为10 L。该条件下的平衡常数为___▲____;
2NH3(g),在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,达到平衡时,N2的转化率为50%,体积变为10 L。该条件下的平衡常数为___▲____;
已知25℃时有关弱电解质的电离平衡常数如下表:
| 弱电解质化学式 | CH3COOH | HCN | H2CO3 | NH3.H2O |
| 电离平衡常数 | 1.8×l0–5 | 4.9×l0–10 | K1=4.3×l0–7 K2=5.6×l0–11 | 1.8×l0–5 |
根据上表中数据回答下列问题:
(1)CH3COO- 、CN- 、CO32-结合质子(即H+)的能力大小顺序_____________________;25℃时,有等浓度的①CH3COONa溶液、②NaCN溶液、③NaHCO3溶液,三种溶液的pH由大到小的顺序为 (填序号)。
(2)Na2CO3水溶液呈碱性的原因,用离子方程式表示: ,
溶液中各离子浓度大小顺序: 。
(3) NaCN溶液中通入少量二氧化碳,反应的离子方程式为
(4)室温下,向盛一定量的稀氨水烧杯中逐滴加入物质的量浓度相同的醋酸,当恰好中和时,溶液的pH 7(填“大于”、“等于”或“小于”)。
(5)甲、乙两瓶氨水的浓度分别为1mol·L-1、0.1mol·L-1,
则c(OH-)甲﹕c(OH-)乙 10(填“大于”、“等于”或“小于”)。
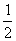 O2(g) = H2O(g) △H=-241.8 kJ/mol ③
O2(g) = H2O(g) △H=-241.8 kJ/mol ③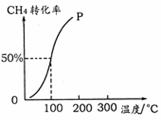 (2)将1.0 mol CH4和2.0 mol H2O ( g )通入容积为100 L的反应室,在一定条件下发生反应:CH4 ( g ) + H2O ( g ) =CO ( g ) + 3H2 ( g ) ,测得在一定的压强下CH4的转化率与温度的关系如右图。
(2)将1.0 mol CH4和2.0 mol H2O ( g )通入容积为100 L的反应室,在一定条件下发生反应:CH4 ( g ) + H2O ( g ) =CO ( g ) + 3H2 ( g ) ,测得在一定的压强下CH4的转化率与温度的关系如右图。
 移向 溶液。
移向 溶液。


 和乙酸酐为原料制备
和乙酸酐为原料制备 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
