在容积固定的容器中发生反应:COg)+2H2g)CH3OHg) ΔH<0,各物质的浓度如表所示:
| 浓度 时间 | cCO)/mol·L-1 | cH2)/mol·L-1 | cCH3OH)/mol·L-1 |
| 0 | 0.8 | 1.6 | 0 |
| 2 min | 0.6 | x | 0.2 |
| 4 min | 0.3 | 0.6 | 0.5 |
| 6 min | 0.3 | 0.6 | 0.5 |
下列说法不正确的是 )。
A.2~4 min内用H2表示的平均反应速率为0.3 mol·L-1·min-1
B.达到平衡时,CO的转化率为62.5%
C.反应在第2 min时改变了条件,可能是加入了催化剂
D.反应在第2 min时改变了条件,可能是增加了H2的浓度
下图是某煤化工产业链的一部分,试运用所学知识,解决下列问题:
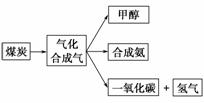
1)已知该产业链中某反应的平衡常数表达式为K=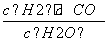 ,它所对应反应的化学方程式是
,它所对应反应的化学方程式是
____________________________________________________。
2)合成甲醇的主要反应是2H2g)+COg)CH3OHg) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度mol·L-1) | 0.2 | 0.1 | 0.4 |
①该时间段内反应速率vH2)=________。
②比较此时正、逆反应速率的大小:v正________v逆填“>”、“<”或“=”)。
③反应达到平衡后,保持其他条件不变,若只把容器的体积缩小一半,平衡 ________填“逆向”、“正向”或“不”)移动,平衡常数K________填“增大”、“减小”或“不变”)。
3)固氮是科学家致力研究的重要课题。自然界中存在天然的大气固氮过程:
N2g)+O2g)===2NOg) ΔH=+180.8 kJ·mol-1,工业合成氨则是人工固氮。
分析两种固氮反应的平衡常数,下列结论正确的是________填字母序号)。
| 反应 | 大气固氮 | 工业固氮温度/℃ | ||||
| 27 | 2 000 | 25 | 350 | 400 | 450 | |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
A.常温下,大气固氮很难进行,而工业固氮却能非常容易进行
B.模拟大气固氮应用于工业上的意义不大
C.工业固氮时温度越低,氮气与氢气反应越完全
D.K越大说明合成氨反应的速率越大
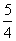 O2g)===
O2g)===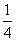 P4O10s)
P4O10s)