直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)吸收液吸收SO2的过程中,pH随n(SO )∶n(HSO
)∶n(HSO )变化关系如下表:
)变化关系如下表:
| n(SO | 91∶9 | 1∶1 | 9∶91 |
| pH | 8.2 | 7.2 | 6.2 |
由上表判断,NaHSO3溶液显________性,用化学平衡原理解释:________________________________________________________________________。
(2)当吸收液的pH降至约为6时,需送到电解槽再生。再生示意图如下:
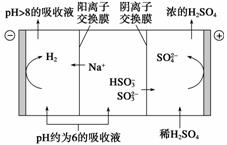
当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:
________________________________________________________________________。
常温下,浓度均为0.1 mol·L-1的6种溶液pH如下:
| 溶质 | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaClO |
| pH | 11.6 | 9.7 | 12.3 | 10.0 | 4.0 | 10.3 |
请根据上表数据回答:
(1)常温下,相同物质的量浓度的下列稀溶液,其酸性由强到弱的顺序是__________(用A、B、C表示)。
A.H2SiO3 B.H2SO3 C.H2CO3
(2)在上述NaHCO3溶液中加0.1 mol·L-1CaCl2,不能产生CaCO3沉淀的原因:________________________________________________________________________。
(3)6种溶液中,水的电离程度最小的是________(填化学式)。
(4)若增大氯水中次氯酸的浓度,可向氯水中加入上表中的物质是________(填化学式)。
(5)等浓度的H2SO3和NaHSO3混合液,加入少量的强酸或强碱溶液,pH值都没有明显变化,请解释之。(用离子方程式表示)_________________________________________________。
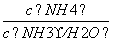 先增大再减小
先增大再减小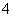 )=c(CH3COO-)
)=c(CH3COO-) 等杂质。某次除杂操作时,往粗盐水中先加入过量的________________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO
等杂质。某次除杂操作时,往粗盐水中先加入过量的________________(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO