人体血液里存在重要的酸碱平衡: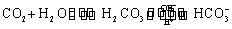 使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随
使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒。其pH随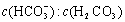 变化关系如下表:
变化关系如下表:
|
| 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.4 | 7.45 |
下列说法不正确的是( )
A.正常人体血液中,HCO3-的水解程度大于电离程度
B.人体血液酸中毒时,可注射NaHCO3溶液缓解
C.pH=7.00的血液中,c(H2CO3)<c(HCO3-)
D.pH=7.40的血液中,HCO3-的水解程度一定大于H2CO3的电离程度
验证周期表中同一周期内从左到右元素的性质的变化规律和同一主族内从上到下的元素性质变化规律: 从下表(Ⅰ)中选择实验方法,从(Ⅱ)中选择相应的实验现象,上下对应地填写在答案的空格中(答错扣1分)。
| 实验方法(Ⅰ) | 实验现象(Ⅱ) | |||||||||
| A.钠与冷水反应 | a.溶液分层,下层变为橙色 | |||||||||
| B.向NaOH溶液中滴加酚酞 | b.产生白烟 | |||||||||
| C.将H2S溶液中通入氯气 | c.反应不十分剧烈,产生的气体能燃烧 | |||||||||
| D.蘸浓氨水与浓盐酸的两玻璃棒接近 | d.浮于水面,熔成小球,迅速向四处游动 | |||||||||
| E.NaI溶液中加入溴水,再加入CCl4 | e.生成白色胶状沉淀,后又溶解 | |||||||||
| F.镁带与沸水反应 | f.产生大量气泡、气体可以点燃 | |||||||||
| G.AlCl3溶液中加入NaOH溶液 | g.溶液变棕黄色 | |||||||||
| H.NaCl溶液中加入溴水 | h.发出耀眼的强光,生成白色物质 | |||||||||
| I.镁带空气中燃烧 | i.溶液出现淡黄色沉淀 | |||||||||
| J.NaBr溶液中加入氯水,再加入CCl4 | j.观察不出什么现象 | |||||||||
| K.铝片与2mnol/L盐酸反应 | k. 溶液分层,下层变为紫色 | |||||||||
| 同周期 | ||||||||||
| Ⅰ | ||||||||||
| Ⅱ | ||||||||||
| 同主族 | ||||||||||
| Ⅰ | ||||||||||
| Ⅱ | ||||||||||
解释在同一周期内从左到右金属性逐渐减弱的原因:
下图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知B、C、D、E在常温下为气体单质,化合物G的颜色反应为黄色,I和 J通常为气态;I和 J相遇产生白烟
同周期 | ||||||
Ⅰ | A | C | F | G(K) | ||
Ⅱ | d | i | C | E(f) | ||
同主族 | ||||||
Ⅰ | E | H | J | |||
Ⅱ | k | j | a |
用化学语言回答下列问题:
(1)A D K
(2) 实验室制C的化学方程式
(3) A 与B反应的方程式:
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
| 族
| IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)④、⑤、⑥的离子半径由大到小的顺序为 。
 (2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是 。
 (3)①、④、⑤中的某些元素可形成既含离子键又含非极性共价键的化合物,写出一种化合物的电子式: 。
(3)①、④、⑤中的某些元素可形成既含离子键又含非极性共价键的化合物,写出一种化合物的电子式: 。
 (4)由表中两种元素的原子按1︰1组成的常见液态化合物的稀溶液易被催化分解,来加快产生常见的某气体;可使用的催化剂为(填序号) _。
(4)由表中两种元素的原子按1︰1组成的常见液态化合物的稀溶液易被催化分解,来加快产生常见的某气体;可使用的催化剂为(填序号) _。
 a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
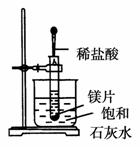 (2)产生上述现象的原因是_____________________________;
(2)产生上述现象的原因是_____________________________; (1)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式:____________________________________________。
(1)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式:____________________________________________。 ”或“=”)。
”或“=”)。