1)已知Na2S2O3 + H2SO4 = Na2SO4 + S↓+ SO2 + H2O 。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下(所取溶液体积均为10mL):
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol·L-1 | c(H2SO4)/mol·L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.1 | 0.2 |
| ③ | 50 | 0.2 | 0.1 |
| ④ | 50 | 0.1 | 0.1 |
其他条件不变时:探究浓度对化学反应速率的影响,应选择____________。(填实验编号);
探究温度对化学反应速率的影响,应选择____________。(填实验编号)。
(2)甲同学设计如下实验流程探究Na2S2O3的化学性质。

(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和____________ 性。
(Ⅱ)生成白色沉淀B的离子方程式是 ____________。
(Ⅲ)已知Na2S2O3溶液与Cl2反应时, 1mol Na2S2O3转移8 mol电子。该反应的离子方程式是____________。
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)⇌2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和如图表示:
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5molA 0.5molB | 1.5molA 0.5molB | 6.0molA 2.0molB |
下列说法正确的是( )

|
| A. | 10min内甲容器中反应的平均速率v(A)=0.025mol/(L•min) |
|
| B. | 由图可知:T1<T2,且该反应为吸热反应 |
|
| C. | x=1,若平衡时保持温度不变,改变容器体积平衡移动 |
|
| D. | T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为75% |
将4.0mol PCl3 和2.0mol Cl2 充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)⇌PCl5(g).达到平衡时,PCl5 为0.80mol,如果此时移走2.0mol PCl3 和l.0mol Cl2,在相同温度下再达平衡时PCl5 的物质的量是( )
|
| A. | 大于0.4 mol,小于0.8 mol | B. | 0.4 mol |
|
| C. | 小于0.4 mol | D. | 0.8 mol |
已知,N2 (g) + 3H2(g) 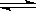 2NH3(g) △H=-92.4 kJ·mol-1 。在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
2NH3(g) △H=-92.4 kJ·mol-1 。在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度(mol·L | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 |
|
|
|
下列说法正确的是
A.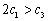 B.
B.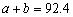 C.
C.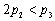 D.α1 +α2 > 1
D.α1 +α2 > 1
 WI2(g)
WI2(g) 


 )
)

