0 141616 141624 141630 141634 141640 141642 141646 141652 141654 141660 141666 141670 141672 141676 141682 141684 141690 141694 141696 141700 141702 141706 141708 141710 141711 141712 141714 141715 141716 141718 141720 141724 141726 141730 141732 141736 141742 141744 141750 141754 141756 141760 141766 141772 141774 141780 141784 141786 141792 141796 141802 141810 203614


 4H++2Fe2++4SO42- ;
4H++2Fe2++4SO42- ;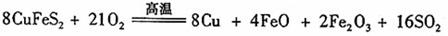
 离子是否存在
离子是否存在