加强空气质量检测,客观分析空气中污染物的来源及性质,将有助于制定有针对性的治理措施。下表是某城市某日的空气质量报告:
| 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 55 | SO2 | II | 良 |
该市某校研究性学习小组对表中首要污染物SO2导致酸雨的成因进行了如下探究:
(1)用下图所示装置进行实验。
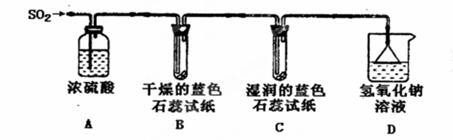
①A装置的作用是____________________。
②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊
试纸变成________________色,说明SO2与水反应生成一种酸,其化学反应方程式是 。
③D装置的作用是__________________________________________________,
D中发生反应的化学方程式是_________________________________________。
(2)往盛有水的烧杯中通入SO2气体,测得所得溶液的pH________7(填“>”“=”或“<”),然后每隔1h测定其pH,发现pH逐渐_______(填“变大”或“变小”), 直至恒定,原因是 (写出反应的离子方程式)。
(3)SO2形成酸雨的另一途径为:SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4, 则在此过程中的飘尘是作为___________(填“催化剂”或“氧化剂”)。
(4)SO2与空气中的氧气、水反应生成硫酸而形成酸雨。该市可能易出现酸雨。
(5)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为__________________,是造成酸雨的另一主要原因。
某研究性学习小组在研究化学反应中的能量变化时,做了下面的实验:

在一个小烧杯里,加入20 g已研磨成粉末的Ba(OH)2·8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10 g NH4Cl晶体,根据实验步骤,填写下表,并回答问题。
| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的 ① 产生 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是 ② 反应 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有 ③ 生成 |
① ② ③
④写出实验过程中发生反应的化学方程式:____________________。
⑤实验中要立即用玻璃棒迅速搅拌的原因是: __________________。
⑥在上述实验过程中,为什么用浸有稀硫酸的湿棉花置于多孔塑料板上?
______________________________________________________。
元素周期律和周期表,揭示了元素之间的内在联系,反映了元素性质与它的原子结构的关系,在哲学、自然科学、生产实践各方面都有重要意义。下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
 |

(1)这8种元素中金属性最强的元素是______(填元素符号或化学式,下同),元素最高价氧化物对应的水化物中酸性最强的酸是______;
(2)元素⑧的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是_________;
(3)③、⑤、⑦三种元素按原子半径由大到小的顺序排列为___________;
 (4)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式______________,______________。若用球棍模型表示①和④形成的化合物的分子结构,应该是___________。
(4)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式______________,______________。若用球棍模型表示①和④形成的化合物的分子结构,应该是___________。
(5)w是第四周期与③同主族的元素。据此推测w不可能具有的性质是
A.最高正化合价为+5价 B.气态氢化物比NH3稳定
C.最高价氧化物的水化物的酸性比硝酸弱 D.单质在常温下可与氢气化合
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
|
|

X溶液与Y溶液反应的离子方程式_______,M中阳离子的鉴定方法____________。


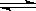 CO2(g)+4H2 (g)
CO2(g)+4H2 (g)
