0 135383 135391 135397 135401 135407 135409 135413 135419 135421 135427 135433 135437 135439 135443 135449 135451 135457 135461 135463 135467 135469 135473 135475 135477 135478 135479 135481 135482 135483 135485 135487 135491 135493 135497 135499 135503 135509 135511 135517 135521 135523 135527 135533 135539 135541 135547 135551 135553 135559 135563 135569 135577 203614

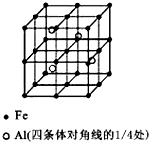 一种Al-Fe合金的立体晶胞如图所示.请据此回答下列问题:
一种Al-Fe合金的立体晶胞如图所示.请据此回答下列问题:





 (1)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,与Ni(CO)n中配体互为等电子体的离子的化学式为
(1)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,与Ni(CO)n中配体互为等电子体的离子的化学式为