题目内容
甲醇可通过将煤的气化中生成的CO和H2在一定条件下发生如下反应得:CO(g)+2H2(g)?CH3OH(g).请根据图回答下列问题:

(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)= .
(2)该反应的热化学方程式CO(g)+2H2(g)?CH3OH(g)△H= .
(3)在恒温恒容条件下,判断该反应达到化学平衡状态的依据是 (填序号);
A.v逆(H2)=2v正(CH3OH) B.v逆(H2)=v正(CO)
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)若在一个体积可变的密闭容器中充入1mol CO、2mol H2和1mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则开始时该反应向 (填“正”、“逆”)反应方向进行,理由是 .

(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=
(2)该反应的热化学方程式CO(g)+2H2(g)?CH3OH(g)△H=
(3)在恒温恒容条件下,判断该反应达到化学平衡状态的依据是
A.v逆(H2)=2v正(CH3OH) B.v逆(H2)=v正(CO)
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)若在一个体积可变的密闭容器中充入1mol CO、2mol H2和1mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则开始时该反应向
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)根据图I时,反应中CO浓度的变化,结合速率公式计算,速率之比等对应物质的计量数之比;
(2)根据反应物与生成物的总能量来分析吸热还是放热,并书写热化学反应方程式,得到△H;
(3)正逆反应速率相等,各物质的浓度不发生变化时表示化学反应处于平衡状态;
(4)同温同压下,混合气体的密度与摩尔质量成正比,如果平衡不移动,密度应相等,据此分析.
(2)根据反应物与生成物的总能量来分析吸热还是放热,并书写热化学反应方程式,得到△H;
(3)正逆反应速率相等,各物质的浓度不发生变化时表示化学反应处于平衡状态;
(4)同温同压下,混合气体的密度与摩尔质量成正比,如果平衡不移动,密度应相等,据此分析.
解答:
解:(1)由图I可知,反应中CO浓度的变化为:1.00-0.25=0.75mol?L-1,则v(CO)=
=
=0.075mol/(L?min),所以v(H2)=2v(CO)=2×0.075mol/(L?min)=0.15mol.L-1.min-1,
故答案为:0.15mol.L-1.min-1;
(2)反应物的总能量为419kJ,生成物的总能量为510kJ,则该反应为放热反应,放出的热量为419kJ-510kJ=91kJ,热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol,
故答案为:-91 kJ/mol;
(3)A.v逆(H2)=2v逆(CH3OH)=2v正(CH3OH),已达平衡状态,故选;
B.v逆(H2)=v正(CO),不等于计量数之比,故不选;
C.容器内压强保持不变,说明气体物质的量不变,已达平衡状态,故选;
D.混合气体的密度保持不变,从反应开始到平衡一直不变,故不选;
故选AC;
(4)同温同压下,混合气体的密度与摩尔质量成正比,如果平衡不移动,密度应相等,现在密度是原来的1.6倍,所以平衡向气体计量数减小的方向移动,故答案为:正,该反应前后气体总质量不变,同温同压下达平衡时气体密度增大,即气体体积缩小,反应正向进行.
| △c |
| t |
| 0.75mol?L |
| 10min |
故答案为:0.15mol.L-1.min-1;
(2)反应物的总能量为419kJ,生成物的总能量为510kJ,则该反应为放热反应,放出的热量为419kJ-510kJ=91kJ,热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol,
故答案为:-91 kJ/mol;
(3)A.v逆(H2)=2v逆(CH3OH)=2v正(CH3OH),已达平衡状态,故选;
B.v逆(H2)=v正(CO),不等于计量数之比,故不选;
C.容器内压强保持不变,说明气体物质的量不变,已达平衡状态,故选;
D.混合气体的密度保持不变,从反应开始到平衡一直不变,故不选;
故选AC;
(4)同温同压下,混合气体的密度与摩尔质量成正比,如果平衡不移动,密度应相等,现在密度是原来的1.6倍,所以平衡向气体计量数减小的方向移动,故答案为:正,该反应前后气体总质量不变,同温同压下达平衡时气体密度增大,即气体体积缩小,反应正向进行.
点评:本题为综合性习题,考查影响化学平衡的因素、热化学反应、化学平衡常数、反应速率的计算,图象的分析和利用等知识点,注重对高考热点知识的考查,是较好的习题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列递变情况中,正确的是( )
| A、Na、Mg、Al原子的最外层电子数依次减少 |
| B、Si、P、S元素的最高正价依次降低 |
| C、C、O、N的原子半径依次减小 |
| D、Li、Na、K的原子半径依次增大 |
科学家根据元素周期律和原子结构理论预测出原子序数为114的元素的存在,下面关于它的原子结构和性质预测不正确的是( )
| A、该元素原子的最外层电子数为4 |
| B、其常见价态为+2、+4 |
| C、它的金属性比铅强 |
| D、它的原子半径比第115号元素的原子半径小 |
下列实验操作和现象中,正确的是( )
| A、在相对过量的氢氧化钠溶液中滴入少量硫酸铜溶液以配制氢氧化铜悬浊液 |
| B、在稀氨水中逐渐加入过量的硝酸银溶液来配制银氨溶液 |
| C、试管里加入少量淀粉,再加入一定量稀硫酸,加热3~4分钟,然后加入银氨溶液,片刻后管壁上有“银镜”出现 |
| D、溴乙烷在氢氧化钠溶液的存在下进行水解后,加入硝酸银溶液,可检验溴离子的存在 |
| E、向较稀的KSCN和FeCl3的混合溶液中加入少量KCl固体,溶液颜色深浅不变 |
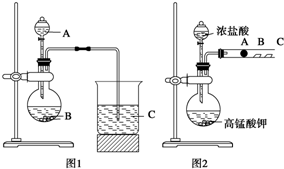 某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律.A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律.A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.
 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答: