0 135001 135009 135015 135019 135025 135027 135031 135037 135039 135045 135051 135055 135057 135061 135067 135069 135075 135079 135081 135085 135087 135091 135093 135095 135096 135097 135099 135100 135101 135103 135105 135109 135111 135115 135117 135121 135127 135129 135135 135139 135141 135145 135151 135157 135159 135165 135169 135171 135177 135181 135187 135195 203614



 2013年冬季,雾霾天气多次肆虐我国东部地区.其中汽车尾气是造成空气污染的原因之一,研究控制汽车尾气成为保护环境的首要任务.
2013年冬季,雾霾天气多次肆虐我国东部地区.其中汽车尾气是造成空气污染的原因之一,研究控制汽车尾气成为保护环境的首要任务.
 )在一定条件下发生缩聚反应,可生成芳香族聚碳酸酯,写出反应的化学方程式
)在一定条件下发生缩聚反应,可生成芳香族聚碳酸酯,写出反应的化学方程式
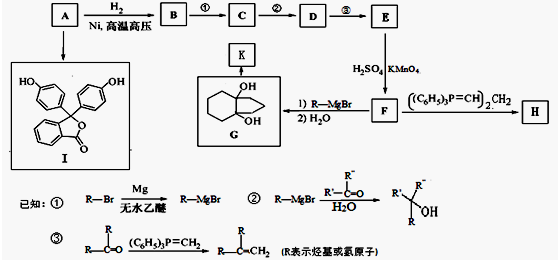
 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
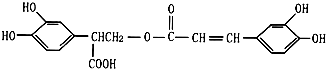
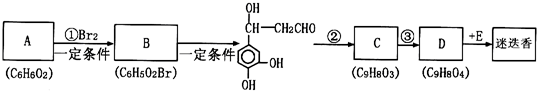

 ;则机理b是
;则机理b是