含有3.01×1024个氧原子的H2SO4的物质的量是( )
| A、0.500mol |
| B、1.00mol |
| C、2.50mol |
| D、1.25mol |
下列说法不正确的是( )
| A、1g氢气在氧气中完全燃烧生成气态水,放出热量120.9kJ,氢气的燃烧热大于241.8kJ?mol-1 | |||
B、500℃30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)
| |||
| C、常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 | |||
| D、已知中和热为-57.3 kJ?mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量要大于57.3 kJ |
NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A、常温常压下,22.4L甲烷含有的共价键数目为4NA |
| B、1mol Cl2与足量Fe反应,转移电子的数目为3NA |
| C、标准状况下,22.4L二氯甲烷含有的分子数目为NA |
| D、常温下,48g O2和O3混合气体所含氧原子数为3NA |
某元素X的气态氢化物化学式为H2X,下面的叙述不正确的是( )
| A、该元素的原子最外层上有6个电子 |
| B、该元素最高价氧化物的化学式为XO3 |
| C、该元素是非金属元素 |
| D、该元素最高价氧化物对应水化物的化学式为H2XO3 |
 如图为周期表中短周期的一部分,若a原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
如图为周期表中短周期的一部分,若a原子最外层电子数比次外层电子数少3,则下列说法正确的是( )| A、a、b、c的最高价氧化物对应水化物的酸性逐渐减弱 |
| B、a的氢化物比c的氢化物稳定 |
| C、a能形成+5价化合物 |
| D、原子半径的大小顺序是a>d>c>b |
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、由水电离的c(H+)=10-4mol/L的溶液中:Fe2+、SO42-、K+、NO3- | ||
| B、由水电离的c(H+)=10-14mol/L的溶液中:Ca2+、Na+、HCO3-、NO3- | ||
C、
| ||
| D、c(Fe3+)=0.1mol/L的溶液中:Na+、K+、NO3-、SO32- |
下列离子方程式书写正确的是( )
| A、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
| B、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| C、NaAlO2溶液中通入足量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D、氢氧化钡溶液与稀硫酸混合:Ba2++SO42-═BaSO4↓ |
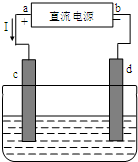 与图有关的下列叙述正确的是( )
与图有关的下列叙述正确的是( )| A、a为直流电源的负极 |
| B、用该装置制白铁(镀锌铁),d为铁电极 |
| C、用该装置精炼铜,d为粗铜电极 |
| D、c、d均为石墨电极电解饱和食盐水时,c电极附近pH升高 |
汽水是CO2的饱和溶液,其中存在如下平衡H2CO3?H++HCO
…①HCO
?H++CO
…②将汽水倒入试管中分别进行下列实验,相应分析结论错误的是( )
- 3 |
- 3 |
2- 3 |
| A、加热、平衡①、②可能都向左移动 |
| B、加入澄清石灰水,平衡①、②均向右移动 |
| C、加入CaCO3悬浊液,CaCO3的溶解平衡向正方向移动 |
| D、通入过量CO2或滴加氯水,溶液PH均减小 |