在给定的四种溶液中,各离子能在该溶液中大量共存并形成无色溶液的是( )
| A、滴加甲基橙试液显红色的溶液:Fe3+、NH4+、Cl-、I- |
| B、pH=1的溶液:Cu2+、Na+、Mg2+、NO3- |
| C、由水电离出来的c(H+)═10-13mol/L的溶液中:K+、HCO3-、Br-、Ba2+ |
| D、NaHSO4溶液中:K+、SO42-、NO3-、Al3+ |
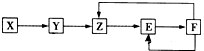 五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如图转化关系,下列推断不合理的是( )
五种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如图转化关系,下列推断不合理的是( )| A、M元素可能是非金属元素,也可能是金属元素 |
| B、X可能是一种氢化物 |
| C、E可能是一种有色气体 |
| D、X→Y可能是非氧化还原反应 |
相同条件下,下列装置中指定电极的电极反应式相同的是( )
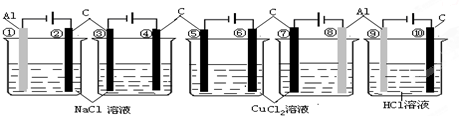

| A、②④⑥⑦⑩ |
| B、①③⑤⑧⑨ |
| C、②③④⑤⑥⑦⑩ |
| D、①③⑤⑦⑨ |
已知甲醇(CH3OH)在常温下为液体,其热值为22.7kJ?g-1,则甲醇的标准燃烧热为( )
| A、-726.4 kJ?mol-1 |
| B、+726.4 kJ?mol-1 |
| C、-1452.8 kJ?mol-1 |
| D、+1452.8 kJ?mol-1 |
2013年诺贝尔化学奖授予将计算模型引入化学反应研究领域的三位科学家,如图是某有机化学反应的一种简单模型(相同的球代表相同原子),推测该反应类型是( )


| A、取代反应 | B、加成反应 |
| C、聚合反应 | D、置换反应 |
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B、在101kPa时,2gH2完全燃料生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ?mol-1 |
| C、由C(石墨,s)=C(金刚石,s)△H=+1.90kJ/mol可知,金刚石比石墨稳定 |
| D、由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol可知,若将含1molCH3COOH的稀溶液与含1mol NaOH的稀溶液混合,放出的热量小于57.3kJ |
短周期元素X、Y、Z、W的原子序数依次增大,其中,X和Z处于同一主族,且Z的单质可与冷水反应生成X的单质,Y元素可分别于X、Z元素形成原子个数比为1:1和1:2的化合物,而W最外层电子数比Y最外层电子数多1个,下列有关说法错误的是( )
| A、简单离子半径大小:W>Y>Z>X |
| B、X、Y和W三种元素可构成六原子分子 |
| C、常温下,X、Y、Z、W的单质均为气体 |
| D、Y与Z可形成既含有离子键又含有共价键的化合物 |
已知2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1 CO(g)+
O2(g)═CO2(g);△H=-282.9kJ?mol-1某H2和CO的混合气体完全燃烧时放出113.74kJ的热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为( )
| 1 |
| 2 |
| A、2:1 | B、1:2 |
| C、1:1 | D、2:3 |
在下列元素中,不属于主族元素的是( )
| A、砷 | B、铍 | C、铁 | D、碘 |
下列叙述正确的是( )
| A、一定温度和压强下,各气态物质体积大小主要由构成气体的分子数决定 |
| B、摩尔质量就是该物质的相对分子质量或相对原子质量 |
| C、单位物质的量的物质所占的体积就是气体摩尔体积 |
| D、40g NaOH溶解在1L水中.形成溶液溶质的物质的量浓度为1mol/L |