题目内容
相同条件下,下列装置中指定电极的电极反应式相同的是( )
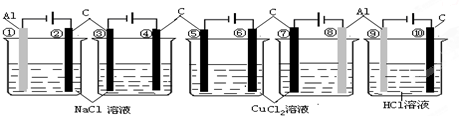

| A、②④⑥⑦⑩ |
| B、①③⑤⑧⑨ |
| C、②③④⑤⑥⑦⑩ |
| D、①③⑤⑦⑨ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该装置均是电解池,活泼电极作阳极时,阳极上电极材料失电子发生氧化反应,惰性电极作阳极时,阴离子在阳极上失电子发生氧化反应;阴极上电解质溶液中阳离子得电子发生还原反应,根据离子放电顺序判断电极上的产物.
解答:
解:该装置均是电解池,①为阴极是氢离子得电子;
②为阳极是氯离子失电子;
③为阴极是氢离子得电子;
④为阳极是氯离子失电子;
⑤阴极是铜离子得电子;
⑥为阳极是氯离子失电子;
⑦为阳极是氯离子失电子;
⑧阴极是铜离子得电子;
⑨为阴极是氢离子得电子;
⑩为阳极是氯离子失电子;
所以电极的电极反应式相同的为②④⑥⑦⑩;
故选A.
②为阳极是氯离子失电子;
③为阴极是氢离子得电子;
④为阳极是氯离子失电子;
⑤阴极是铜离子得电子;
⑥为阳极是氯离子失电子;
⑦为阳极是氯离子失电子;
⑧阴极是铜离子得电子;
⑨为阴极是氢离子得电子;
⑩为阳极是氯离子失电子;
所以电极的电极反应式相同的为②④⑥⑦⑩;
故选A.
点评:本题考查电解池原理,明确阴阳极上离子的放电顺序是解本题关键,注意活泼电极作阳极时阳极上发生的电极反应,为易错点,题目难度不大.

练习册系列答案
相关题目
下面说法正确的是( )
| A、摩尔是七个基本物理量之一 |
| B、摩尔是物质的量的单位 |
| C、物质的量就是物质的质量 |
| D、阿伏加德罗常数就是6.02×1023 |
三聚氰胺,分子式C3H6N6.是一种用途广泛的基本有机化工中间产品.动物长期摄入三聚氰胺会造成生殖、泌尿系统的损害,膀胱、肾部结石,并可进一步诱发膀胱癌.有毒的三鹿牌奶粉就是因为其牛奶和奶粉中添加三聚氰胺,以提升食品检测中的蛋白质含量指标.下列关于三聚氰胺的说法中你认为正确的是( )
| A、三聚氰胺之所以被不法分子加入奶粉中,就是因为其蛋白质含量较高的原因 |
| B、三聚氰胺的中碳、氢、氮三种元素的质量比为12:1:14 |
| C、每摩尔三聚氰胺分子中含有原子个数为15NA(用NA表示阿伏德罗常数的值) |
| D、三聚氰胺的摩尔质量为126 |
已知2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1 CO(g)+
O2(g)═CO2(g);△H=-282.9kJ?mol-1某H2和CO的混合气体完全燃烧时放出113.74kJ的热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为( )
| 1 |
| 2 |
| A、2:1 | B、1:2 |
| C、1:1 | D、2:3 |
关于2mol二氧化碳的叙述中,正确的是( )
| A、体积为44.8L |
| B、含有4mol原子 |
| C、分子数为6.02×1023 |
| D、质量为88g |
设NA为阿伏加德罗常数的值.下列叙述不正确的是( )
| A、7.80g Na2O2与5.85g NaCl所含阴离子数均为0.1NA |
| B、常温常压下,22.4L NH3所含分子数小于NA |
| C、一定条件下,1.4g N2与0.2mol H2混合充分反应,转移的电子数为0.3NA |
| D、标准状况下,28g聚乙烯完全燃烧,产生的CO2数为2NA |
能正确表示下列反应的离子方程式是( )
| A、足量硫化氢气体通入硫酸铁溶液中:H2S+Fe3+═Fe2++S↓+2H+ |
| B、足量铁与稀硝酸反应:Fe+4H++NO3-═Fe2++2H2O+NO↑ |
| C、醋酸溶液与纯碱反应:CO32-+2H+═H2O+CO2↑ |
| D、等物质的量的Ba(OH)2与NaHSO4在溶液中反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
“高钙牛奶”、“含氟牙膏”、“铁强化酱油”等商品名称中的“钙”、“氟”、“铁”指的是( )
| A、单质 | B、元素 | C、分子 | D、氧化物 |
