物质的分类依据通常有组成和性质,下列对钠的化合物的分类的说法中,只考虑组成的是( )
| A、Na2O2是氧化物,不是碱性氧化物 |
| B、Na2CO3不是碱,是一种钠盐 |
| C、NaOH是一元碱、强碱 |
| D、NaClO是氧化性盐、含氧酸盐 |
已知有如下反应:
①2BrO
+Cl2=Br2+2ClO
,
②ClO
+5C1-+6H+=3Cl2+3H2O,
③2FeCl3+2Kl=2FeCl+2KCl+l2
④2FeCl2+Cl2=2FeCl3.
下列各微粒氧化能力由强到弱的顺序正确的是( )
①2BrO
|
|
②ClO
|
③2FeCl3+2Kl=2FeCl+2KCl+l2
④2FeCl2+Cl2=2FeCl3.
下列各微粒氧化能力由强到弱的顺序正确的是( )
A、ClO
| ||||||||||||||
B、BrO
| ||||||||||||||
C、BrO
| ||||||||||||||
D、BrO
|
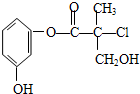 某有机物是药物生产的中间体,其结构简式为下列有关叙述正确的是( )
某有机物是药物生产的中间体,其结构简式为下列有关叙述正确的是( )| A、该有机物与Br2水发生加成反应 |
| B、该有机物与浓硫酸混合加热可发生消去反应 |
| C、该有机物经催化氧化后能发生银镜反应 |
| D、1 mol该有机物与足量NaOH溶液反应最多消耗3 mol NaOH |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B、欲配置1.00mol?L-1的NaCl溶液1.00L,可将溶于1.00L水中 |
| C、1molAl3+离子含有的核外电子数为3NA |
| D、1.0L1.0mo1?L -1 的NaOH水溶液中含有的氧原子数为2NA |
50mL的BaCl2溶液中所含有的Cl-可以被20mL 0.5mol?L-1的AgNO3溶液全部沉淀,则BaCl2溶液中Ba2+的物质的量浓度为( )
| A、1mol?L-1 |
| B、0.8mol?L-1 |
| C、0.2mol?L-1 |
| D、0.1mol?L-1 |
金属的下列性质中,不能用金属的电子气理论加以解释的是( )
| A、易导电 | B、易导热 |
| C、有延展性 | D、易锈蚀 |
下列溶液中有关物质的量浓度关系不正确的是( )
| A、pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有c(NaOH)<c(NaHCO3)<c(CH3COONa) |
| B、已知25℃时Ksp (AgCl)=1.8×10-10,则在0.3mol?L-1NaCl溶液中,Ag+的物质的量浓度最大可达到6.0×10-10mol?L-1 |
| C、25℃时,0.1mol?L-1Na2CO3溶液中水电离出来的c(OH-)大于0.1mol?L-1NaOH溶液中水电离出来的c(OH-) |
| D、室温下,0.1mol?L-1NaHA溶液的pH=4,则有c(HA-)>c(H+)>c(H2A)>c(A2-) |
下列离子方程式正确的是( )
| A、明矾溶于水产生Al(OH)3胶体:Al3++3H2O=Al(OH)3↓+3H+ | ||||
| B、双氧水加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O | ||||
C、用铜做电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| D、Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O |
微量元素是指在人体中含量低于0.01%的元素,这些元素对人体的正常发育和健康起着重要作用,下列各组元素全部是微量元素的是( )
| A、Na、O | B、I、Fe |
| C、O、C | D、H、N |
下列化学应用中不涉及氧化还原反应的是( )
| A、工业上由硅的氧化物制备硅单质 |
| B、生活中使用明矾净水,除去水中的悬浮的微小颗粒 |
| C、漂白粉用作疫区的环境消毒 |
| D、过氧化钠用作呼吸面具的供氧剂 |