分类是化学学习和研究的常用手段.下列分类依据和结论都正确的是( )
| A、HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
| B、H2O、CH3COOH、CaCO3均含有氧元素,都是氧化物 |
| C、HCl、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D、HNO3、浓硫酸都具有强氧化性,都是氧化性酸 |
下列有关叙述正确的是( )
| A、氢键是一种特殊化学键,它广泛地存在于自然界中 |
B、在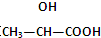 分子中含有1个手性C原子 分子中含有1个手性C原子 |
| C、碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子 |
| D、含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大 |
美国化学家研制出一种新型液态储氢材料,名叫硼氮-甲基环戊烷,它能在室温下安全工作,且在空气和水中也能保持稳定,这项技术进步为科学家们攻克现今制约氢经济发展的氢储存和运输难题提供了解决方案.下列说法正确的是( )
| A、该材料中只存在极性共价键 |
| B、其储氢与放氢过程中只发生物质的变化 |
| C、组成硼氮--甲基环戊烷的四种元素中氮的第一电离能最大 |
| D、甲基环戊烷核磁共振氢谱有3种峰,且峰面积比为3:4:4 |
用酸性氢氧燃料电池为电源进行电解的实验装置如图所示,下列说法正确的是( )

| A、燃料电池工作时,正极反应为:O2+2H2O+4e-═4OH- |
| B、在溶液中SO42-往b极移动 |
| C、若a、b极都是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
| D、若a极是铜,b极是铁时,a极逐渐溶解,b极上有铜析出 |
已知第二周期和第三周期元素形成的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A、离子半径:C3->D->B+>A2+ |
| B、原子序数:d>c>b>a |
| C、原子半径:A>B>D>C |
| D、原子的最外层电子数目:A>B>D>C |
下列性质比较中不正确的是( )
A、沸点的高低: |
| B、熔点:SiO2>CsCl>CBr4>CF4 |
| C、硬度:镁>铝>镁铝合金 |
| D、水溶性:HF>Br2 |
联氨被亚硝酸氧化可生成HN3,化学方程式为N2H4+HNO2═HN3+2H2O.下列说法正确的是( )
| A、HN3只是氧化产物,且分子中存在极性键和非极性键 |
| B、联氨常温下为液态,是因为N2H4分子间存在氢键 |
| C、每生成2mol H2O,反应中转移电子的物质的量一定为4mol |
| D、联氨(N2H4)分子中σ键和π键个数比为2:1 |
氯化铝溶液加热蒸干灼烧得到的固体主要成分是( )
| A、AlCl3 |
| B、Al(OH)3 |
| C、Al2O3 |
| D、Al |
酸、碱完全中和时,有关说法正确的是( )
| A、溶液一定呈中性 |
| B、酸和碱的物质的量一定相等 |
| C、酸和碱的物质的量浓度相等 |
| D、酸能提供的H+与碱能提供的OH-的物质的量相等 |
下列判断错误的是( )
| A、熔点:SiO2>NaCl>SiCl4 |
| B、稳定性:AsH3>PH3>NH3 |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |