用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、25℃时,pH=12的1.0 L NaClO溶液中水电离出OH-的数目为0.01 NA |
| B、标准状况下,22.4 L甲醇中含有的氧原子数为1.0 NA |
| C、0.1 mol乙醇中含有0.6 NA个C-H共价键 |
| D、常温、常压下,3.5 g 35Cl2所含中子数为0.1 NA |
利用化石燃料开采、加工过程产生的H2S废气通过电化学法制取氢气的工艺如图,下列说法不正确的是( )


| A、反应池中的离子方程式:2Fe3++S2-=2Fe2++S↓ | ||||
| B、该工艺优点之一是FeCl3溶液可循环利用 | ||||
| C、电解池中惰性电极C1为阳极 | ||||
D、电解池总反应的化学方程式:2FeCl2+2HCl
|
下列有关说法正确的是( )
| A、BaSO3(s)+4C(s)═BaS(s)+4CO(g)室温下不能自发进行,说明该反应的△H>0 |
| B、H2的热值为142.9kJ?g-1,则氢气燃烧的热化学方程式可表示为2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ?mol-1 |
| C、增大反应物浓度,可增大单位体积内活化分子百分数,从而增加有效碰撞的次数 |
| D、0.1mol?L-1Na2CO3溶液在35℃时碱性比25℃强,说明盐类水解反应是放热反应 |
用NaHCO3和KHCO3组成的混合物分别与三份相同浓度的盐酸进行反应,测得数据如下:
判断下列结论中不正确的是( )
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
| A、混合物中NaHCO3和KHCO3的质量比为1:1 |
| B、加入9.2g混合物时消耗HCl 0.1mol |
| C、盐酸物质的量浓度为3.0mol/L |
| D、15.7g混合物与盐酸反应后有剩余 |
下列实验操作正确的是( )
| A、稀释浓硫酸时,常把水加入到盛浓硫酸的烧杯中 |
| B、不慎将NaOH浓溶液沾到皮肤上,立即用盐酸清洗 |
| C、酒精灯着火时可用水扑灭 |
| D、制取蒸馏水时,为了防止瓶内产生暴沸现象,应先向烧瓶内加入几片碎瓷片 |
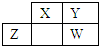 四种短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,Y、Z质子数之和为20,下列说法中不正确的是( )
四种短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,Y、Z质子数之和为20,下列说法中不正确的是( )| A、X、Y、Z、W均为非金属元素 |
| B、X、Y、W的氢化物中,Y的氢化物沸点最高 |
| C、Z的阳离子与Y的阴离子电子层结构相同 |
| D、W元素的简单离子半径大于Z元素的简单离子半径 |
由无水醋酸钠与碱石灰共热可得到甲烷.你预测将无水苯乙酸钠与碱石灰共热时,所得的有机物主要是( )
| A、苯 | B、甲苯 |
| C、乙苯 | D、苯甲酸钠与甲烷 |
下列说法正确的是( )
| A、物质的量就是一定体积的物质的质量 |
| B、阿伏加德罗常数就是6.02×1023 |
| C、钠的摩尔质量等于它的相对原子质量 |
| D、在标准状况下,1 mol 任何气体的体积都约为22.4 L |
近来据报道日本周边海洋发现丰富的稀土资源,下列有关稀土元素
Gd的说法正确的是( )
152 64 |
| A、质子数为152 |
| B、中子数为88 |
| C、质量数为216 |
| D、核外电子数为88 |
下列溶液中溶质的物质的量浓度最接近1mol?L-1的是( )
| A、将58.5 g NaCl溶解于1 L水中配成的溶液 |
| B、将80 g SO3溶于920g水并配成溶液 |
| C、将0.5 mol?L-1的NaNO3溶液100 mL加热蒸发掉50 g水的溶液 |
| D、0.5L K+浓度为4 mol/L的K2SO4溶液加水稀释到1L. |