题目内容
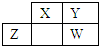 四种短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,Y、Z质子数之和为20,下列说法中不正确的是( )
四种短周期元素X、Y、Z、W在元素周期表中的相对位置如表所示,Y、Z质子数之和为20,下列说法中不正确的是( )| A、X、Y、Z、W均为非金属元素 |
| B、X、Y、W的氢化物中,Y的氢化物沸点最高 |
| C、Z的阳离子与Y的阴离子电子层结构相同 |
| D、W元素的简单离子半径大于Z元素的简单离子半径 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由短周期元素X、Y、Z、W在元素周期表中的位置,可知X、Y处于第二周期,Z、W处于第三周期,令Y的原子序数为a,则Z的原子序数为a+6,Y、Z质子数之和为20,则a+a+6=20,解得a=7,故Y为N元素、X为C元素、Z为Al、W为P元素,据此解答.
解答:
解:由短周期元素X、Y、Z、W在元素周期表中的位置,可知X、Y处于第二周期,Z、W处于第三周期,令Y的原子序数为a,则Z的原子序数为a+6,Y、Z质子数之和为20,则a+a+6=20,解得a=7,故Y为N元素、X为C元素、Z为Al、W为P元素,
A.Z为金属元素Al,其它三种元素为非金属性元素,故A错误;
B.X、Y、W的氢化物中,Y的氢化物分子之间存在氢键,其沸点最高,故B正确;
C.Al3+离子与N3-离子核外电子数都是10,二者电子层结构相同,故C正确;
D.P3-离子电子层比Al3+离子多一个电子层,故离子半径P3->Al3+,故D正确,
故选A.
A.Z为金属元素Al,其它三种元素为非金属性元素,故A错误;
B.X、Y、W的氢化物中,Y的氢化物分子之间存在氢键,其沸点最高,故B正确;
C.Al3+离子与N3-离子核外电子数都是10,二者电子层结构相同,故C正确;
D.P3-离子电子层比Al3+离子多一个电子层,故离子半径P3->Al3+,故D正确,
故选A.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,注意理解掌握同主族元素原子序数关系.

练习册系列答案
相关题目
关于苯分子结构的下列说法中正确的是( )
| A、苯分子中含有3个碳碳双键和3个碳碳单键 |
| B、苯分子为正六边形,每个氢原子垂直于碳原子所在的平面 |
| C、苯环上的碳碳键是一种介于碳碳双键和碳碳单键之间的独特的键 |
| D、苯分子中没有共价单键 |
室温下,某溶液中由水电离出的H+和OH-物质的量浓度乘积为1×10-28,该溶液中一定不能大量共存的是( )
| A、Cl-、AlO2-、K+、Na+ |
| B、Fe2+、NO3-、Ba2+、Cl- |
| C、Fe3+、SO42-、MnO4-、Na+ |
| D、Na+、K+、CO32-、SO42- |
已知A、B、C、D是短周期中原子序数依次增大的4种主族元素,其中元素A、C为处于同主族的非金属元素,其单质在常温下都呈固态.元素B的原子最外层电子数与电子层数相等,元素D在同周期元素中非金属性最强.下列说法正确的是( )
| A、原子半径:A<B<C<D |
| B、气态氢化物的稳定性:D>C |
| C、最高价氧化物对应水化物的酸性:A<C |
| D、常温下单质B能溶于浓硫酸 |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、25℃时,pH=12的1.0 L NaClO溶液中水电离出OH-的数目为0.01 NA |
| B、标准状况下,22.4 L甲醇中含有的氧原子数为1.0 NA |
| C、0.1 mol乙醇中含有0.6 NA个C-H共价键 |
| D、常温、常压下,3.5 g 35Cl2所含中子数为0.1 NA |
下列说法正确的是( )
A、H2O电子式为: |
| B、稳定性:NH3<PH3<AsH3 |
| C、离子半径:Cl->S2->Al3+ |
| D、碱性:Be(OH)2>Mg(OH)2>Al(OH)3 |
下列不能证明醋酸是弱酸的是( )
| A、0.1mol?L-1醋酸的PH为3.1 |
| B、在醋酸溶液中滴加几滴石蕊试液,再加入醋酸钠固体红色变浅 |
| C、醋酸钠溶液的PH>7 |
| D、醋酸溶液中加入氯化钠不反应 |
下列叙述正确的是( )
| A、0.1 mo1?L-1一氨水中,c(OH-)=c(NH4+) |
| B、在常温下,10mL 0.02mo1?L-1的HCl溶液与10mL0.02 mL mo1.L-1的Ba(OH)2溶液 充分混合,若混合后溶液的体积为20mL,则溶液的pH=11 |
| C、在0.1 mol?L-1CH3COONa溶液中,c(OH一)=c(CH3COOH)+c(H+) |
| D、0.1 mo1?L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2 c(A2-)+c(HA)+c(H2 A) |