0 133732 133740 133746 133750 133756 133758 133762 133768 133770 133776 133782 133786 133788 133792 133798 133800 133806 133810 133812 133816 133818 133822 133824 133826 133827 133828 133830 133831 133832 133834 133836 133840 133842 133846 133848 133852 133858 133860 133866 133870 133872 133876 133882 133888 133890 133896 133900 133902 133908 133912 133918 133926 203614
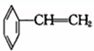 ②
② ③
③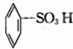 ④
④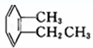 ⑤
⑤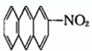
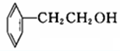 ⑦
⑦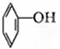 ⑧CH3CH=CH-COOH⑨
⑧CH3CH=CH-COOH⑨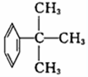
 乙醇分子中不同的化学键如下图①-⑤所示,按乙醇在各种不同反应中断裂的键的位置,将键号填入空格中;书写化学方程式时,有机物必须书写结构简式:
乙醇分子中不同的化学键如下图①-⑤所示,按乙醇在各种不同反应中断裂的键的位置,将键号填入空格中;书写化学方程式时,有机物必须书写结构简式: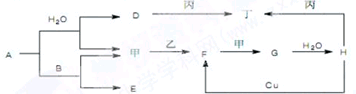
 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.