PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素的原子序数依次增大.X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,W单质是人类将太阳能转变为电能的常用材料.下列说法正确的是( )
| A、X2Y的沸点比X2R高,是因为X2Y分子之间氢键比X2R分子之间的氢键强 |
| B、W与Y形成化合物的分子式为WY2 |
| C、WX4空间构型为正四面体形,WX4分子的稳定性强于甲烷 |
| D、原子半径按Z、W、R、Y、X的顺序依次减小 |
某反应A(g)+3B(g)═2C(g),以下反应速率的表示中最快的是( )
| A、VA=0.4 mol/(L?S) |
| B、VB=0.8 mol/(L?S) |
| C、Vc=0.6 mol/(L?S) |
| D、无法比较 |
X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期.下列说法错误的是( )
| A、气态氢化物稳定性:HmW>HnR |
| B、Y和Z形成的某种化合物中含离子键、非极性健 |
| C、Y、Z、R三者形成的某种化合物溶于水后,可形成碱性溶液 |
| D、标准状况下,1mol XW4的体积约为22.4L |
某盐酸的物质的量浓度为12.0mol/L,其密度为1.19g/cm3,现有该浓度的盐酸100mL,则用于吸收HCl气体形成该盐酸的水的体积为( )
| A、75.2mL |
| B、85.5mL |
| C、90.8mL |
| D、100mL |
 常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应.根据图象下列说法不正确的是( )
常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应.根据图象下列说法不正确的是( )| A、比较b、c、d三点时的溶液中,水电离的c(OH-)大小顺序:d>c>b | ||
B、滴定时,由b点到c点的过程中,
| ||
| C、点b所示溶液中:c(NH4+)+c(H+)>c(NH3.H2O)+c(OH-) | ||
| D、若某温度下,pH=11的NH3?H2O和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3?H2O与NH3三种微粒的平衡浓度之和为0.1mol?Lˉ1 |
下列装置图及有关说法正确的是( )
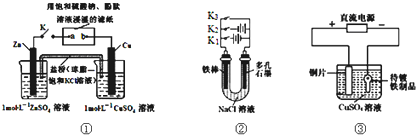

| A、装置①中K键闭合时,片刻后CuSO4溶液中c(Cl-)增大 |
| B、装置①中K键闭合时,片刻后可观察到滤纸a点变红色 |
| C、装置②中铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>只闭合K2>都断开 |
| D、装置③中当铁制品上析出1.6g铜时,电源负极输出的电子数为0.025NA |
下列物质不属于有机物的是( )
| A、碳酸 | B、汽油 | C、蔗糖 | D、酒精 |
海水中可以提取镁,其方法是首先使海水中的Mg2+转化为Mg(OH)2沉淀.从经济效益的角度考虑,可在海水中加入的物质是( )
| A、NaOH |
| B、KOH |
| C、CaO |
| D、Na2O |
对于可逆反应2A+3B?2C;△H<0,下列条件的改变一定可以加快正反应速率的是( )
| A、增加压强 |
| B、升高温度 |
| C、增加A的量 |
| D、加入二氧化锰作催化剂 |
对于任何一个可逆反应,同时影响化学反应速率和化学平衡的因素是( )
①催化剂 ②浓度 ③压强 ④温度.
①催化剂 ②浓度 ③压强 ④温度.
| A、只有②③④ | B、只有②④ |
| C、只有④ | D、全部 |