用价层电子对互斥理论预测CO32-和BF3的立体结构分别是( )
| A、平面三角形;三角锥形 |
| B、三角锥形;平面三角形 |
| C、三角锥形;三角锥形 |
| D、平面三角形;平面三角形 |
常温下,下列关于电解质溶液的正确判断是( )
| A、pH=11的NaOH溶液中c(H+)是pH=9的Ba(OH)2溶液中c(H+)的100倍 |
| B、使甲基橙变红的溶液中,K+、NO3-、SO32-、HCO3-可以大量共存 |
| C、由0.1 mol?L-1一元酸HA溶液的pH=1,可推知HA溶液存在HA?H++A- |
| D、由0.1 mol?L-1一元碱MOH溶液的pH=10,可推知MCl溶液pH<7 |
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A、1 mol碳正离子(CH+3)所含的电子总数为8NA | ||
| B、1 mol甲基(-CH3)所含的电子总数为9NA | ||
| C、0.5 摩1,3-丁二烯分子中含有C=C双键数为 NA | ||
D、标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为
|
下列说法中正确的是( )
| A、乙炔分子中,每个碳原子都有两个未杂化的2p轨道形成π键 |
| B、sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道 |
| C、凡中心原子采取sp2杂化的分子,其分子构型都是平面三角形 |
| D、凡AB2型的共价化合物,其中心原子A均采用sp杂化轨道成键 |
已知下列热化学方程式:2H2O(g)═2H2(g)+O2(g)△H=+483.6kJ/mol,2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol.当1g水由液态变为气态时,其热量变化是( )
①吸热 ②放热 ③2.44kJ ④88kJ.
①吸热 ②放热 ③2.44kJ ④88kJ.
| A、①④ | B、②④ | C、①③ | D、②③ |
用石墨电极电解NaBr的水溶液时,下列叙述不正确的是( )
| A、电解时阳极得到Br2,阴极得到NaOH和H2 |
| B、若取阳极附近的溶液中滴入淀粉溶液,溶液呈蓝色 |
| C、若取阴极附近的溶液中滴入酚酞试液,溶液变红色 |
| D、若取阳极附近的溶液少量于试管中,滴入少量的苯,振荡静置后上层溶液呈橙红色 |
配制物质的量浓度为0.1mol?L-1的Na2CO3溶液100mL时,下列操作正确的是( )
| A、用托盘天平称取1.06g无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中 |
| B、在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水 |
| C、定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分 |
| D、定容时,若仰视,则所配溶液的浓度将偏高 |
用固体氯化钠配制浓度为1.00mol/L的氯化钠溶液100mL,用不到的仪器是( )
| A、托盘天平 | B、容量瓶 |
| C、玻璃棒 | D、试管 |
某溶液中加入铝粉,有H2放出,在该溶液中一定能大量共存的离子组是( )
| A、K+、Mg2+、Cl-、SO42- |
| B、Na+、NH4+、SO42-、HCO3- |
| C、Na+、K+、SO42-、Cl- |
| D、K+、Na+、NO3-、AlO2- |
下列关于图的实验装置说法正确的是( )
A、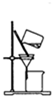 该图装置可以提纯精制氢氧化铁胶体 |
B、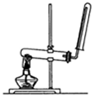 该图装置可以用来制备和收集氨气和氧气 |
C、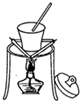 该图可以从食盐水中得到食盐晶体 |
D、 该图试管中放新制FeSO4溶液,从滴管中滴加NaOH溶液,易于观察到Fe(OH)2颜色 |