题目内容
用石墨电极电解NaBr的水溶液时,下列叙述不正确的是( )
| A、电解时阳极得到Br2,阴极得到NaOH和H2 |
| B、若取阳极附近的溶液中滴入淀粉溶液,溶液呈蓝色 |
| C、若取阴极附近的溶液中滴入酚酞试液,溶液变红色 |
| D、若取阳极附近的溶液少量于试管中,滴入少量的苯,振荡静置后上层溶液呈橙红色 |
考点:电解原理
专题:电化学专题
分析:A、电解池的阳极上发生失电子的氧化反应,根据放电顺序确定放电的离子;
B、根据阳极上的电极反应确定产物,根据产物的性质确定现象;
C、电解池的阳极上发生得电子的还原反应,根据放电顺序确定放电的离子以及产物;
D、根据阳极上的电极反应确定产物,根据产物的性质确定现象.
B、根据阳极上的电极反应确定产物,根据产物的性质确定现象;
C、电解池的阳极上发生得电子的还原反应,根据放电顺序确定放电的离子以及产物;
D、根据阳极上的电极反应确定产物,根据产物的性质确定现象.
解答:
解:用石墨电极电解NaBr的水溶液时,阳极上电极反应:2Br--e-=Br2,阴极上电极反应:2H++2e-=H2↑.
A、根据两极反应知道:电解时阳极得到Br2,阴极得到NaOH和H2,故A正确;
B、阳极上电极反应:2Br--e-=Br2,若取阳极附近的溶液中滴入淀粉溶液,溶液不会显蓝色,碘单质遇到淀粉变蓝,溴单质没有该性质,故B错误;
C、阴极得到NaOH和H2,若取阴极附近的溶液中滴入酚酞试液,溶液变红色,故C正确;
D、阳极上电极反应:2Br--e-=Br2,若取阳极附近的溶液少量于试管中,滴入少量的苯,振荡静置后会出现萃取分层现象,溴单质溶解于苯中,上层溶液呈橙红色,故D正确.
故选B.
A、根据两极反应知道:电解时阳极得到Br2,阴极得到NaOH和H2,故A正确;
B、阳极上电极反应:2Br--e-=Br2,若取阳极附近的溶液中滴入淀粉溶液,溶液不会显蓝色,碘单质遇到淀粉变蓝,溴单质没有该性质,故B错误;
C、阴极得到NaOH和H2,若取阴极附近的溶液中滴入酚酞试液,溶液变红色,故C正确;
D、阳极上电极反应:2Br--e-=Br2,若取阳极附近的溶液少量于试管中,滴入少量的苯,振荡静置后会出现萃取分层现象,溴单质溶解于苯中,上层溶液呈橙红色,故D正确.
故选B.
点评:本题考查电解工作原理,题目较简单,根据电解质溶液中离子移动方向判断电极是关键.

练习册系列答案
相关题目
下列物质属于非电解质的是( )
| A、BaSO4 |
| B、Cl2 |
| C、CH3COOH |
| D、CCl4 |
“物质的量”是联系宏观世界和微观世界的桥梁.下列说法正确的是( )
| A、“摩尔”是“物质的量”的单位 |
| B、1 mol O2的质量是32 g/mol |
| C、任何气体的“气体摩尔体积”均为22.4 L/mol |
| D、10 mL 2 mol/L H2SO4溶液中取出的5 mL溶液,其浓度为1 mol/L |
下列说法中不正确的是( )
| A、1 mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L |
| B、1 mol臭氧和1.5 mol氧气含有相同的氧原子数 |
| C、浓度均为1 mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1 |
| D、等物质的量的干冰和葡萄糖(C6H12O6)中所含碳原子数之比为1:6,氧原子数之比为1:3 |
用价层电子对互斥理论预测CO32-和BF3的立体结构分别是( )
| A、平面三角形;三角锥形 |
| B、三角锥形;平面三角形 |
| C、三角锥形;三角锥形 |
| D、平面三角形;平面三角形 |
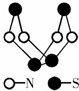 如图是已经合成的最著名硫-氮化合物分子结构.下列说法正确是( )
如图是已经合成的最著名硫-氮化合物分子结构.下列说法正确是( )| A、该物质的分子式为SN |
| B、该物质中的N原子最外层都达到8电子稳定结构 |
| C、该物质的分子中既有极性键又有非极性键 |
| D、该物质与化合物S2N2互为同素异形体 |
在室温下,pH相同、体积相同的氨水和氢氧化钠溶液,采取下列措施后,有关叙述正确的是( )
| A、温度下降20℃,两溶液的pH均不变 |
| B、各加水稀释10倍,两溶液的pH仍相等 |
| C、分别加入适量的氯化铵晶体,两溶液的pH均减小 |
| D、各用相同物质的量浓度的盐酸中和,所消耗盐酸的体积相等 |
将氮气、一氧化碳、二氧化碳的混合气体先通过足量澄清石灰水,再通过足量灼热的氧化铜,最后剩余的气体是( )
| A、氮气 | B、二氧化碳 |
| C、一氧化碳 | D、二氧化碳和氮气 |
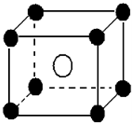 某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点,阴离子Y(○)位于立方体的中心,试分析:
某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点,阴离子Y(○)位于立方体的中心,试分析: