用1L 1.0mol/L NaOH溶液吸收0.8mol C02,所得溶液中含有( )
| A、C032- |
| B、HC03- |
| C、C032-和HC03- |
| D、C032-和OH- |
下列说法中不正确的是( )
| A、二十碳五烯酸和二十二碳六烯酸是鱼油的主要成分,它们含有相同的官能团,是同系物,化学性质相似 |
B、结构简式为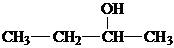 的有机物其名称为 2-丁醇 的有机物其名称为 2-丁醇 |
| C、分子式为C4H8Br2结构中含一个一CH3的同分异构体(不考虑立体异构)有4种 |
D、某有机物球棍结构模型为: ,则该有机物能发生消去反应和氧化反应 ,则该有机物能发生消去反应和氧化反应 |
短周期元素A、B、C,原子序数依次递增.已知:A、C同主族,而且三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述中正确的是( )
| A、A、B形成的化合物中含有共价键 |
| B、沸点:A的氢化物高于C的氢化物 |
| C、离子半径:A<B<C |
| D、电负性:C>B>A |
可证明次氯酸为弱酸的事实是( )
| A、有漂白性 |
| B、可与碱发生反应 |
| C、能见分解 |
| D、次氯酸钙与水、二氧化碳反应生成次氯酸 |
一定温度下,可逆反应N2(g)+3H2(g)?2NH3(g) 达到平衡状态标志的是( )
| A、A、B、C的分子数之比为1:3:2 |
| B、单位时间内生成amol N2,同时生成amolNH3 |
| C、每断裂1molN≡N,同时断裂3molH-H |
| D、每生成1mol N≡N,同时生成6molN-H |
设NA代表阿伏加德罗常数,下列有关叙述正确的是( )
| A、1mol甲烷分子所含质子数、电子数均为10NA |
| B、1L0.1mol/L乙酸溶液中的H+离子数为0.1NA |
| C、24g镁原子最外层电子数为NA |
| D、标准状况下,22.4L乙醇的分子数等于NA |
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、100 mL 2.0 mol?L-1 NH4Cl溶液中含有NH4+的数目为0.2NA |
| B、25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA |
| C、标准状况下,2.24L庚烷含有的分子数为0.1NA |
| D、常温常压下,NO2与足量H2O反应生成0.1molNO,则转移的电子数为0.2NA |
人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,服用维生素C可以解毒.对上述事实分析不正确的是( )
| A、亚硝酸盐是氧化剂 |
| B、维生素C是氧化剂 |
| C、亚硝酸盐将Fe3+还原成Fe2+ |
| D、维生素C被Fe3+氧化 |
下列装置或操作错误,不能达到实验目的是( )
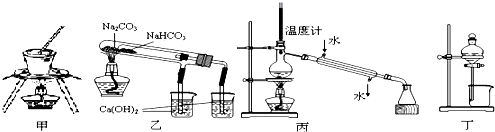

| A、用甲图装置可用于加热、灼烧固体 |
| B、用乙图装置验证NaHCO3和Na2CO3的热稳定性 |
| C、用丙图装置分离乙醇与水 |
| D、用丁图装置可由四氯化碳萃取碘水中的碘 |
下列说法不正确的是( )
| A、核磁共振仪、红外光谱仪、质谱仪、紫外光谱仪、元素分析仪、紫外可见分光光度计等都是定性或定量研究物质组成或结构的现代仪器 |
| B、利用元素周期律,人们在过渡元素中寻找各种性能优良的催化剂,使反应的温度降低并提高反应物的转化率,从而起到很好的节能效果 |
| C、化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础 |
| D、垃圾焚烧法已成为许多城市垃圾处理的主要方法之一,利用垃圾焚烧产生的热能发电或供热,能较充分的利用生活垃圾中的生物质能 |