下列反应原理不符合工业冶炼金属实际情况的是( )
A、2HgO
| ||||
B、2NaCl(熔融)
| ||||
C、2MgO(熔融)
| ||||
D、Fe2O3+3CO
|
下列叙述正确的是( )
| A、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出 |
| B、用托盘天平准确称取5.85克NaCl |
| C、氢氧化钠溶液保存在带玻璃塞的试剂瓶中 |
| D、用广泛PH试纸测得0.10mol/LNH4Cl溶液的PH=5.2 |
某温度下,反应H2(g)+I2(g)?2HI(g);(正反应为放热反应).在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是( )
| A、恒容,充入H2,I2百分含量降低 |
| B、恒温,压缩体积,平衡不移动,颜色加深 |
| C、恒容,升温,正反应速率减小 |
| D、恒压,充入HI,开始时正反应速率减小 |
能正确表示下列反应的离子反应方程式为( )
| A、NH4HCO3溶于少量的浓KOH溶液中:NH4++HCO3-+2OH-═CO32-+NH3↑+2 H2O |
| B、磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O |
| C、FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 |
| D、H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
用NA表示阿伏加德罗常数,下列叙述不正确的是( )
| A、常温常压下,18gH2O含电子数为10NA |
| B、标准状况下,22.4L氦气含有的原子数为NA |
| C、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
| D、48gO2和 O3的混合物所含的氧原子数为3NA |
下列说法正确的是( )
| A、纤维素属于髙分子化合物,与淀粉互为同分异构体,水解后均生成葡萄糖 |
| B、2,3一二甲基丁烷的H一NMR上有5个峰 |
| C、含5个碳原子的有机物,每个分子中最多可形成4个C一C单键 |
D、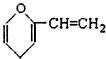 某有机物结构如图所示,该有机物属于芳香族化合物的同分异构体有5种,其中遇FeCl3能显色的有3种 |
实现下列变化时,需克服相同类型作用力的是( )
| A、二氧化硅和干冰的熔化 |
| B、液溴和液汞的汽化 |
| C、金刚石和冰的熔化 |
| D、碘和干冰的熔化 |
下列离子方程式正确的是( )
| A、FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O | ||||
| B、过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | ||||
C、H
| ||||
| D、向氯化铝溶液中滴加过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
甲、乙两烧杯中各盛有200mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入的铝粉质量为( )
| A、10.8g | B、7.2g |
| C、2.7g | D、1.8g |
下列有关金属的说法正确的是( )
| A、用坩埚钳夹住铁丝在酒精灯上加热红热,迅速伸进氧气瓶中,燃烧火星四射,放出大量的热,生成红棕色的固体 |
| B、相同物质的量的钠在常温和加热的条件下与氧气反应所得的产物不同,但转移的电子数相同. |
| C、钠可以与冷水反应生成碱和氢气,铁必须与水蒸气反应才能生成碱和氢气 |
| D、等物质的量的铝分别与足量的盐酸和NaOH溶液反应生成相同条件下 氢气的体积比为1:3 |