通过下列实验得出的结论,其中正确的是( )

①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成的
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水是由氢元素、氧元素组成,又说明了水分子中氢原子和氧原子个数之比为2:1
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低
⑤既可说明二氧化碳易溶于水,又说明了二氧化碳具有酸性.

①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成的
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水是由氢元素、氧元素组成,又说明了水分子中氢原子和氧原子个数之比为2:1
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低
⑤既可说明二氧化碳易溶于水,又说明了二氧化碳具有酸性.
| A、①②③④ | B、②③④⑤ |
| C、②③④ | D、①②③④⑤ |
下列说法不正确的是( )
| A、化学反应是旧键断裂和新键形成的过程 |
| B、盖斯定律实质上是能量守恒定律的体现 |
| C、反应前后分子数不变遵循的是质量守恒定律 |
| D、溶解平衡、水解平衡和电离平衡均为动态平衡 |
下列实验没有问题的是( )
A、 实验室制乙炔 |
B、 实验室制乙烯 |
C、 实验室制溴苯 |
D、 除去乙烷中的乙烯 |
在t℃时,向2L密闭容器中放入1molA和1molB,发生下列反应:A(g)+B(g)?C(g)+2D(g),平衡时C的含量为m%,保持其他条件不变,若按下列配比将物质放入容器中达到平衡时,C的含量仍为m%的是( )
| A、2molA和1molB |
| B、2molD和A、B、C各1mol |
| C、1molC和2molD |
| D、1molC和1molD |
下列说法中正确的是( )
| A、物质发生化学反应不一定都伴随着能量变化 |
| B、只要有能量变化的物质变化都是化学反应 |
| C、化学反应中生成物的总能量一定低于反应物的总能量 |
| D、化学反应中反应物的总能量与生成物的总能量一定不同 |
一定条件下,a g某物质在足量的O2中充分燃烧后,将其产物全部通入足量的Na2O2固体中,反应后固体质量恰好也增加了a g,下列物质中不能满足上述结果的是( )
| A、CH4 |
| B、CH3COOH |
| C、CO |
| D、H2 |
下列图示与对应的叙述相符的是( )
A、 说明烯烃与H2的加成反应是放热反应,虚线表示在有催化剂的条件下进行 |
B、 用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由图曲线可确定①的酸性最强 |
C、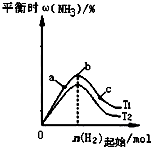 图表示合成氨反应在其他条件不变的情况下,改变n(H2)起始对平衡的影响.由此可知,N2的转化率最高的是b点;且T1>T2,K2>K1(T1和T2表示温度,K1、K2表示对应温度下的平衡常数) |
D、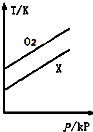 在体积相同的两个密闭容器中,分别充入等质量的O2和X气体,由图可确定X可能是CH4 |
下列为制取溴苯实验的有关现象的叙述和解释,其中正确的是( )
| A、实验室制取的溴苯的实验后液体呈褐色,由于产物溴苯是褐色的 |
| B、溴苯比水轻,因此溴苯浮在水面上 |
| C、实验室制取溴苯时,导管口出现白雾,是由于HBr遇水蒸气而形成的 |
| D、溴苯和苯的混合物可以用水萃取分离 |
能正确表示下列反应的离子方程式是( )
| A、Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-═2Fe2++I2+3H2O | ||||
| B、铝粉与NaOH的D2O溶液反应:2Al+2OH-+2D2O═2AlO2-+H2↑+2D2↑ | ||||
| C、5.6g Fe与200mL 2.0 mol/L HNO3溶液充分反应:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O | ||||
D、三氯化铁浓溶液滴入沸水中,制取氢氧化铁胶体Fe3++3H2O
|
高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是 ( )
| A、浓硝酸 | B、硝酸银 |
| C、氯水 | D、纯碱 |