下列说法正确的是( )
| A、常温下Na与足量的氧气反应生成Na2O,随温度升高生成Na2O的速率加快 |
| B、常温下pH=9的CH3COONa溶液和pH=9的NH3?H2O溶液,两溶液中水电离的c(H+)之比为104:1 |
| C、凡是放热反应都是自发进行的反应,而吸热反应都是非自发进行的反应 |
| D、pH=13的强碱溶液,加水稀释后,溶液中所有离子的浓度均变小 |
下列有关摩尔质量的描述或应用中,不正确的是( )
A、1 mol NH
| ||
| B、SO2的摩尔质量为64 g?mol-1 | ||
| C、铝原子的摩尔质量等于它的相对原子质量 | ||
D、一个水分子的质量约等于
|
碳纳米管是近年来材料科学研究的热点.为除去碳纳米管中的杂质--碳纳米颗粒(少量碳原子的聚集体),可以将样品溶解于强酸性的K2Cr2O7溶液中充分反应,当溶液由橙色转变为墨绿色(Cr3+)即可,同时放出一种无毒的气体.以下判断正确的是( )
| A、可以用浓盐酸调节K2Cr2O7溶液的酸性 |
| B、该过程中每氧化2 mol碳纳米颗粒,转移8NA个电子 |
| C、若将该反应设计为原电池,则碳纳米颗粒应作为原电池的正极 |
| D、可以通过过滤的方法最终得到碳纳米管 |
下列实验装置或操作(已略去部分夹持仪器)正确的是( )
A、 配置溶液 |
B、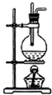 实验室制乙烯 |
C、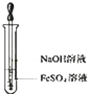 制备Fe(OH)2 |
D、 制备与收集氨气 |
某温度下,氯化镁饱和溶液浓度为40%,在足量的此溶液中加入4.6g无水氯化镁,最终析出结晶水合物40.6g,则该结晶水合物的化学式是( )
| A、MgCl2?7H2O |
| B、MgCl2?2H2O |
| C、MgCl2?6H2O |
| D、MgCl2?5H2O |
下列叙述不合理的是( )
| A、用SO2漂白品红溶液,加热溶液又恢复红色 |
| B、用带玻璃塞的玻璃试剂瓶盛装NaOH溶液 |
| C、用食醋清洗暖瓶中的水垢 |
| D、用铁制或铝制容器运输浓硫酸 |
固体碘在受热时发生升华现象,有关叙述正确的是( )
| A、碘受热升华,破坏的是分子间作用力,未破坏I-I共价键,因此未发生吸热反应 |
| B、碘受热升华,吸收热量,发生了吸热反应 |
| C、碘升华,未破坏共价键,不供应热量也能发生 |
| D、碘升华过程中,热能转变为化学能 |
下列说法正确的是( )
| A、胆矾是电解质、液氨是非电解质 |
| B、淀粉溶液、硅酸、氯化铁溶液均为胶体 |
| C、淀粉、纤维素、油脂都属于天然高分子化合物 |
| D、SO3、SiO2、NO2均为酸性氧化物 |
下列对于“摩尔”的理解正确的是( )
| A、摩尔是国际科学界建议采用的一种物理量 |
| B、摩尔是物质的量的单位,简称摩,符号为mol |
| C、22.4LO2中所含氧气分子计量为1摩尔 |
| D、1mol氧含6.02×1023个O2 |
五种短周期的原子半径及主要化合价如表,下列叙述不正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.104 | 0.111 | 0.066 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、L、T形成的化合物的晶体类型与M、T形成的化合物的晶体类型相同 |
| B、工业生产中L、M的单质均用电解其熔融盐的方法冶炼而得 |
| C、相同条件下,等物质的量的单质与氢气化合放出能量:T>Q |
| D、离子半径:Q2->T2->L2+>M3+ |