题目内容
下列叙述不合理的是( )
| A、用SO2漂白品红溶液,加热溶液又恢复红色 |
| B、用带玻璃塞的玻璃试剂瓶盛装NaOH溶液 |
| C、用食醋清洗暖瓶中的水垢 |
| D、用铁制或铝制容器运输浓硫酸 |
考点:二氧化硫的化学性质,硅和二氧化硅,铝的化学性质,铁的化学性质
专题:元素及其化合物
分析:A.二氧化硫漂白具有暂时性;
B.玻璃塞中的二氧化硅与NaOH反应生成具有粘合性的硅酸钠;
C.水垢的成分为碳酸钙,与醋酸可反应;
D.常温下,Fe、Al遇浓硫酸发生钝化.
B.玻璃塞中的二氧化硅与NaOH反应生成具有粘合性的硅酸钠;
C.水垢的成分为碳酸钙,与醋酸可反应;
D.常温下,Fe、Al遇浓硫酸发生钝化.
解答:
解:A.二氧化硫漂白具有暂时性,则用SO2漂白品红溶液,加热溶液又恢复红色,故A正确;
B.玻璃塞中的二氧化硅与NaOH反应生成具有粘合性的硅酸钠,不能选玻璃塞,故B错误;
C.水垢的成分为碳酸钙,与醋酸可反应,则用食醋清洗暖瓶中的水垢,故C正确;
D.常温下,Fe、Al遇浓硫酸发生钝化,生成致密的氧化膜阻止反应的进一步发生,则用铁制或铝制容器运输浓硫酸,故D正确;
故选B.
B.玻璃塞中的二氧化硅与NaOH反应生成具有粘合性的硅酸钠,不能选玻璃塞,故B错误;
C.水垢的成分为碳酸钙,与醋酸可反应,则用食醋清洗暖瓶中的水垢,故C正确;
D.常温下,Fe、Al遇浓硫酸发生钝化,生成致密的氧化膜阻止反应的进一步发生,则用铁制或铝制容器运输浓硫酸,故D正确;
故选B.
点评:本题考查物质的性质,综合考查元素化合物知识,为高频考点,涉及知识点较多,综合性强,较好的训练学生的思维转换及解决问题的能力,注意性质与现象、用途的关系,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验不能达到预期目的是( )
| A、用饱和碳酸钠溶液除去乙酸乙酯中混有的乙酸 |
| B、向某溶液中滴入稀盐酸与氯化钡的混合溶液,检验该溶液中是否含有SO42- |
| C、将颗粒大小相同的钠与钾分别与水反应,比较钠、钾金属活泼性的强弱 |
| D、将Mg(OH)2和Al(OH)3分别与过量NaOH溶液反应,比较其碱性的强弱 |
设NA为阿伏加德罗常数的值,下列判断正确的是( )
| A、1 mol/LAlCl3溶液,含有Al3+的数目为NA |
| B、标准状况下,22.4LCCl4中分子数目为NA |
| C、0.1mol Fe与过量的稀硫酸充分反应,转移的电子数为0.3 NA |
| D、O2和O3组成的48g混合气体中含有3 NA个氧原子 |
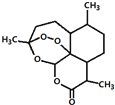 2011年9月23日,中国科学家屠呦呦获得了美国拉斯克医学奖的临床医学奖,获奖理由是“因为发现青蒿素--一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.如图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )
2011年9月23日,中国科学家屠呦呦获得了美国拉斯克医学奖的临床医学奖,获奖理由是“因为发现青蒿素--一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.如图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )| A、青蒿素分子式为C15H22O5 |
| B、青蒿素有-O-O-键具有较强的氧化性 |
| C、青蒿素易溶于水、乙醇、苯 |
| D、青蒿素在碱性条件下易发生水解反应 |
NH3的共轭酸是( )
| A、NH4+ |
| B、NH2- |
| C、NH2- |
| D、HCONH2 |
下列说法正确的是( )
| A、常温下Na与足量的氧气反应生成Na2O,随温度升高生成Na2O的速率加快 |
| B、常温下pH=9的CH3COONa溶液和pH=9的NH3?H2O溶液,两溶液中水电离的c(H+)之比为104:1 |
| C、凡是放热反应都是自发进行的反应,而吸热反应都是非自发进行的反应 |
| D、pH=13的强碱溶液,加水稀释后,溶液中所有离子的浓度均变小 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、明矾溶液:K+、Cl-、HCO3-、OH- |
| B、pH=7的溶液中:Fe3+、Mg2+、NO3-、SO42- |
| C、弱碱性的溶液中:K+、Ca2+、SiO32-、HCO3- |
| D、能使pH试纸变深红色的溶液中:Na+、NH4+、I-、SO42- |
一定温度下,某密闭容器中发生如下反应:2X(g)+Y(s)?2Z(g),确实达到平衡的标志是( )
| A、X的生成速率与Z的消耗速率数值相等 |
| B、X、Y、Z的浓度之比为2:1:2 |
| C、体积一定时,容器内压强不再变化 |
| D、体积一定时,混合气体的密度不再变化 |
下列事实中,能说明氯的非金属性比硫强的是( )
| A、次氯酸的氧化性比稀硫酸强 |
| B、氯化氢比硫化氢的热稳定性好 |
| C、高氯酸(HClO4)的酸性比硫酸强 |
| D、氯原子最外层电子数比硫原子的多 |