25℃时,下列液体的pH大于7的是( )
| A、蒸馏水 | B、人的胃液 |
| C、醋酸钠溶液 | D、氯化铵溶液 |
向含下列离子的溶液中分别加入NaOH固体(溶液体积不变),能引起离子浓度减小的是( )
| A、Cl- |
| B、OH- |
| C、AlO2- |
| D、HCO3- |
下列反应既属于离子反应,又属于氧化还原反应的是( )
| A、BaCl2溶液与K2SO4溶液混合 |
| B、CuSO4溶液与NaOH溶液混合 |
| C、Zn放入稀H2SO4中 |
| D、KSCN溶液与FeCl3溶液混合 |
常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如图所示:下列有关说法正确的是( )
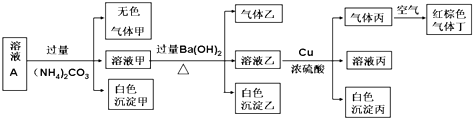

| A、沉淀乙一定有BaCO3,可能有BaSO4 |
| B、实验消耗Cu 14.4g,则生成气体丁的体积为3.36L |
| C、该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子 |
| D、生成的甲、乙、丙气体均为无色的易溶于水气体 |