题目内容
I、已知反应:
3I-(aq)+S2O82-(aq)?I3-(aq)+2SO42-(aq);
(1)写出反应的平衡常数表达式K= .
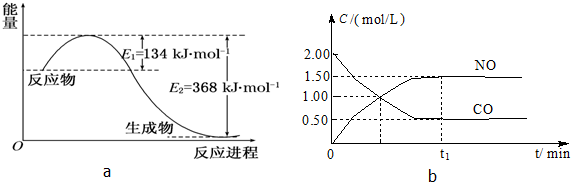
(2)图1表示反应过程中有关物质的能量,则反应的△H 0(填>、<、=).
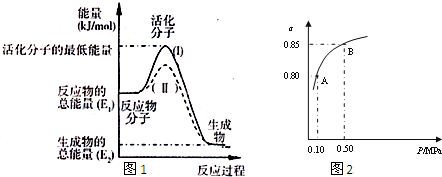
(I)、(II)两线中,使用催化剂的是 线.
(3)反应中发生反应的I-与被氧化的I-的物质的量比为 .
(4)反应的速率可以用I3-与加入的淀粉溶液反应是蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃进行实验,记录的数据如下:
则:该实验的目的是 显色时间t1= s分析表中数据,得出的结论是
II、二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)
2SO3(g)某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示.
根据图2所示回答下列问题.
①平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”、“=”).
②已知上述反应的是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列选项中有利于提高SO2平衡转化率的有 (填字母).A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 F.移出氧气.
3I-(aq)+S2O82-(aq)?I3-(aq)+2SO42-(aq);
(1)写出反应的平衡常数表达式K=
(2)图1表示反应过程中有关物质的能量,则反应的△H

(I)、(II)两线中,使用催化剂的是
(3)反应中发生反应的I-与被氧化的I-的物质的量比为
(4)反应的速率可以用I3-与加入的淀粉溶液反应是蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃进行实验,记录的数据如下:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol?L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-/mol?L-1) | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
II、二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)
| 催化剂 |
| △ |
根据图2所示回答下列问题.
①平衡状态由A变到B时,平衡常数K(A)
②已知上述反应的是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列选项中有利于提高SO2平衡转化率的有
考点:用化学平衡常数进行计算,反应热和焓变,化学平衡的影响因素,化学平衡的计算
专题:基本概念与基本理论
分析:Ⅰ、(1)化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值;
(2)根据反应物和产物能量的相对大小确定反应的吸放热情况;使用催化剂可以降低反映的活化能,加快反应速率;
(3)氧化还原反应中,化合价升高的元素被氧化,据此回答;
(4)由题目中表格数据可分析出c(I-)、c(S2O32-)浓度越大,反应速率越快,显蓝色所需时间越少,故实验目的应是研究反应物I-与S2O82-的浓度对反应速率的影响;
对比数据组①和②、数据组②和③、数据组③和④、数据组①和③,分析当其中一个变量(即一种反应物浓度)保持不变时,反应时间的变化(即反应速率的变化),然后分析当两个变量同时变化一定的倍数时,反应时间的变化(即反应速率的变化),就可以得出其中的规律,据此计算t1.
Ⅱ、①平衡常数只受温度的影响,温度不变,则K不变;
②从外界条件对平衡移动的影响分析.
(2)根据反应物和产物能量的相对大小确定反应的吸放热情况;使用催化剂可以降低反映的活化能,加快反应速率;
(3)氧化还原反应中,化合价升高的元素被氧化,据此回答;
(4)由题目中表格数据可分析出c(I-)、c(S2O32-)浓度越大,反应速率越快,显蓝色所需时间越少,故实验目的应是研究反应物I-与S2O82-的浓度对反应速率的影响;
对比数据组①和②、数据组②和③、数据组③和④、数据组①和③,分析当其中一个变量(即一种反应物浓度)保持不变时,反应时间的变化(即反应速率的变化),然后分析当两个变量同时变化一定的倍数时,反应时间的变化(即反应速率的变化),就可以得出其中的规律,据此计算t1.
Ⅱ、①平衡常数只受温度的影响,温度不变,则K不变;
②从外界条件对平衡移动的影响分析.
解答:
解:(1)化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,则3I-(aq)+S2O82-(aq)?I3-(aq)+2SO42-(aq);
的化学平衡常数为K=
,故答案为:
;
(2)根据图中信息知道:反应物的能量高于产物的能量,所以反应是放热的,即焓变小于零,使用催化剂可以降低反映的活化能,加快反应速率,即为图中的曲线(Ⅱ),故答案为:<;(Ⅱ);
(3)反应中发生反应的I-为3mol,根据电子转移是2mol,只有2mol碘离子被氧化,发生反应的I-与被氧化的I-的物质的量比为3:2,故答案为:3:2;
(4)由题目中表格数据可分析出c(I-)、c(S2O32-)浓度越大,反应速率越快,显蓝色所需时间越少,故实验目的应是研究反应物I-与S2O82-的浓度对反应速率的影响.
对比数据组①和②、③和④,可以看到,c (S2O82-)不变,c (I-)增大到2倍时,反应时间缩短了一半,即反应速率加快了一倍;
对比数据组②和③,可以看到,c (I-)不变,c (S2O82-)增大到2倍时,反应时间缩短了一半,即反应速率也加快了一倍;
对比数据组对比数据组①和③,可以看到,c (I-)和c (S2O82-)均增大到2倍时,反应时间为原反应时间的1/4,即反应速率加快了4倍.
可见两个反应物的浓度和反应速率之间的数学关系是:反应物浓度每增加一倍,反应时间就减少一倍,对于两个反应物来说都是如此,
可得出结论:反应速率与反应物起始浓度乘积成正比.
对比实验①和⑤,实验⑤的c (I-)为实验①的4倍,而c (S2O82-)保持不变,则由此可计算实验⑤的反应时间应为实验①反应时间的1/4,即t1=88s×
=22s.
故答案为:研究反应物I-与S2O82-的浓度对反应速率的影响;22s;反应速率与反应物起始浓度乘积成正比;
Ⅱ、①平衡常数只受温度的影响,温度不变,则K不变,平衡状态由A变到B时,则k(A)=k(B),故答案为:=;
②反应放热,为提高SO2平衡转化率,应使平衡向正反应方向移动,可降低温度,体积不变,不能从压强的角度考虑,催化剂不影响平衡移动,移出氧气,平衡向逆反应方向移动,不利于提高SO2平衡转化率,
故答案为:B.
的化学平衡常数为K=
| c(I3-)?c2(SO42-) |
| c3(I-)?c(S2O82-) |
| c(I3-)?c2(SO42-) |
| c3(I-)?c(S2O82-) |
(2)根据图中信息知道:反应物的能量高于产物的能量,所以反应是放热的,即焓变小于零,使用催化剂可以降低反映的活化能,加快反应速率,即为图中的曲线(Ⅱ),故答案为:<;(Ⅱ);
(3)反应中发生反应的I-为3mol,根据电子转移是2mol,只有2mol碘离子被氧化,发生反应的I-与被氧化的I-的物质的量比为3:2,故答案为:3:2;
(4)由题目中表格数据可分析出c(I-)、c(S2O32-)浓度越大,反应速率越快,显蓝色所需时间越少,故实验目的应是研究反应物I-与S2O82-的浓度对反应速率的影响.
对比数据组①和②、③和④,可以看到,c (S2O82-)不变,c (I-)增大到2倍时,反应时间缩短了一半,即反应速率加快了一倍;
对比数据组②和③,可以看到,c (I-)不变,c (S2O82-)增大到2倍时,反应时间缩短了一半,即反应速率也加快了一倍;
对比数据组对比数据组①和③,可以看到,c (I-)和c (S2O82-)均增大到2倍时,反应时间为原反应时间的1/4,即反应速率加快了4倍.
可见两个反应物的浓度和反应速率之间的数学关系是:反应物浓度每增加一倍,反应时间就减少一倍,对于两个反应物来说都是如此,
可得出结论:反应速率与反应物起始浓度乘积成正比.
对比实验①和⑤,实验⑤的c (I-)为实验①的4倍,而c (S2O82-)保持不变,则由此可计算实验⑤的反应时间应为实验①反应时间的1/4,即t1=88s×
| 1 |
| 4 |
故答案为:研究反应物I-与S2O82-的浓度对反应速率的影响;22s;反应速率与反应物起始浓度乘积成正比;
Ⅱ、①平衡常数只受温度的影响,温度不变,则K不变,平衡状态由A变到B时,则k(A)=k(B),故答案为:=;
②反应放热,为提高SO2平衡转化率,应使平衡向正反应方向移动,可降低温度,体积不变,不能从压强的角度考虑,催化剂不影响平衡移动,移出氧气,平衡向逆反应方向移动,不利于提高SO2平衡转化率,
故答案为:B.
点评:本题通过陌生情景考查平衡常数、反应中能量变化、氧化还原反应、化学反应速、影响化学反应速率的外界因素(浓度)、学生对图表的观察、分析以及学生对实验数据的分析、整理、归纳等方面的思维能力,难度较大.(4)中解决该类试题应注意:①认真审题,明确实验目的,理解直接测量与实验目的间的逻辑和数学关系;②理解控制变量的思想在实验设计和数据分析中的运用.

练习册系列答案
相关题目
与 互为同分异构体的是( )
互为同分异构体的是( )
 互为同分异构体的是( )
互为同分异构体的是( )A、 |
B、 |
C、 |
D、 |
下列无色有毒的气体是( )
| A、氯气 | B、氟气 |
| C、一氧化碳 | D、二氧化硫 |
已知c(NH4Cl)<0.1mol?L-1时,溶液的pH>5.1,现用0.1mol?L-1盐酸滴定10mL 0.05mol?L-1氨水,用甲基橙作指示剂,达到终点时所用盐酸的量应是( )
| A、10 mL |
| B、5 mL |
| C、大于5 mL |
| D、小于5 mL |
25℃时,下列液体的pH大于7的是( )
| A、蒸馏水 | B、人的胃液 |
| C、醋酸钠溶液 | D、氯化铵溶液 |
下列说法正确的是( )
| A、弱电解质的电离过程是吸热过程 |
| B、升高温度可以抑制盐类的水解 |
| C、正盐水溶液pH均为7 |
| D、硫酸钠水溶液pH小于7 |
 如图,Ⅰ是恒压密闭容器,Ⅱ是恒容刚性密闭容器.其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)?aZ(g).则Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )
如图,Ⅰ是恒压密闭容器,Ⅱ是恒容刚性密闭容器.其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?)?aZ(g).则Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是( )| A、若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ<Ⅱ |
| B、若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ |
| C、若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间相同 |
| D、平衡时Ⅰ容器的体积小于V L |