下列事实不能用勒夏特列原理(平衡移动原理)解释的是( )
①氯化铁溶液加热蒸干最终得不到氯化铁固体;
②铁在潮湿的空气中容易生锈;
③实验室可用排饱和食盐水的方法收集氯气;
④保存FeCl2溶液时向溶液中加入少量铁粉
⑤钠与氯化钾共融制备钾Na(L)+KCl(L)?K(g)+NaCl(L);
⑥二氧化氮与四氧化二氮的平衡体系,加压缩小体积后颜色加深.
①氯化铁溶液加热蒸干最终得不到氯化铁固体;
②铁在潮湿的空气中容易生锈;
③实验室可用排饱和食盐水的方法收集氯气;
④保存FeCl2溶液时向溶液中加入少量铁粉
⑤钠与氯化钾共融制备钾Na(L)+KCl(L)?K(g)+NaCl(L);
⑥二氧化氮与四氧化二氮的平衡体系,加压缩小体积后颜色加深.
| A、①②③ | B、②④⑥ |
| C、③④⑤ | D、②⑤⑥ |
某有机物结构为: ,用系统命名法得到的名称是( )
,用系统命名法得到的名称是( )
 ,用系统命名法得到的名称是( )
,用系统命名法得到的名称是( )| A、2-乙基丙烷 |
| B、2-甲基丁烷 |
| C、3-甲基丁烷 |
| D、新戊烷 |
下列说法正确的是( )
| A、用金属活动性顺序可解释反应:Na(l)+KCl(l)═NaCl(l)+K(g) |
| B、用玻璃棒蘸取某溶液滴在pH试纸上,可测得的溶液pH=2.9 |
| C、在100 mL容量瓶中溶解4.0 g NaOH,可得到1.0 mol/L的NaOH溶液 |
| D、由水的离子积常数Kw随温度升高而增大的事实,可判断水电离是吸热过程 |
在固定容积的密闭容器中合成氨的反应达到了平衡,容器中含有0.1mol N2、0.3mol H2、0.1mol NH3,若维持原来的条件,向该容器中再加入0.1mol N2、0.3mol H2、0.1mol NH3,则( )
| A、正、逆反应速率同时增大,平衡不移动 |
| B、正、逆反应速率同时增大,NH3的百分含量升高 |
| C、正、逆反应速率同时增大,平衡向逆反应方向移动 |
| D、正、逆反应速率不变,平衡不移动 |
 如图所示,在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气的成分仍不变.则钠和氧化汞的物质的量之比是( )
如图所示,在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气的成分仍不变.则钠和氧化汞的物质的量之比是( )| A、1:1 |
| B、2:1 |
| C、23:216.6 |
| D、216.6:23 |
下列图示与对应的叙述相符的是( )

| A、图①可表示将SO2气体通入溴水时pH的变化 |
| B、图②表示KNO3的溶解度曲线,a点是80℃的KNO3的不饱和溶液 |
| C、图③表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D、根据图④,除去CuSO4溶液中Fe3+,可加氨水调节pH=4 |
在一定温度下,可逆反应:X(气)+3Y(气)?2Z(气)达到反应限度的是( )
| A、X、Y、Z的浓度相等 |
| B、X、Y、Z的分子数比为1:3:2 |
| C、Z的生成速率是X的生成速率的二倍 |
| D、单位时间内生成n mol X,同时生成3n mol Y |
下列选用的相关仪器符合实验要求的是( )
A、 存放浓硫酸 |
B、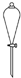 分离水和乙酸乙酯 |
C、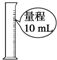 准确量取9.50mL |
D、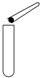 取金属颗粒 |
