题目内容
在一定温度下,可逆反应:X(气)+3Y(气)?2Z(气)达到反应限度的是( )
| A、X、Y、Z的浓度相等 |
| B、X、Y、Z的分子数比为1:3:2 |
| C、Z的生成速率是X的生成速率的二倍 |
| D、单位时间内生成n mol X,同时生成3n mol Y |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、各物质浓度相同不能说明反应达到平衡状态,故A错误;
B、X、Y、Z的分子数比为1:3:2,不是不变,故不能说明物质浓度不变,故B错误;
C、Z的生成速率等效于X的消耗速率的二倍,正逆反应速率相等,故C正确;
D、未体现正逆之间的关系,都反映的是逆反应,故D错误;
故选C.
B、X、Y、Z的分子数比为1:3:2,不是不变,故不能说明物质浓度不变,故B错误;
C、Z的生成速率等效于X的消耗速率的二倍,正逆反应速率相等,故C正确;
D、未体现正逆之间的关系,都反映的是逆反应,故D错误;
故选C.
点评:本题考查了化学平衡状态的分析判断,化学反应速率的影响因素分析,平衡移动原理是解题关键,题目较简单.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
将Na2O2投入FeCl2溶液中,可观察到的现象是( )
| A、生成白色沉淀、有气泡产生 |
| B、生成浅绿色沉淀、有气泡产生 |
| C、生成红褐色沉淀、有气泡产生 |
| D、没有沉淀生成 |
下列物质存放方法错误的是( )
| A、金属钠存放于煤油中 |
| B、FeSO4溶液存放在加有少量铁粉的试剂瓶中 |
| C、氯水置于棕色试剂瓶避光保存 |
| D、将1mol/L的NaCl溶液保存在容量瓶中 |
在固定容积的密闭容器中合成氨的反应达到了平衡,容器中含有0.1mol N2、0.3mol H2、0.1mol NH3,若维持原来的条件,向该容器中再加入0.1mol N2、0.3mol H2、0.1mol NH3,则( )
| A、正、逆反应速率同时增大,平衡不移动 |
| B、正、逆反应速率同时增大,NH3的百分含量升高 |
| C、正、逆反应速率同时增大,平衡向逆反应方向移动 |
| D、正、逆反应速率不变,平衡不移动 |
下列实验现象的描述错误的是( )
| A、新制氯水使紫色石蕊试液变红 |
| B、向NaHCO3固体加入新制氯水,有无色气体产生 |
| C、向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,呈血红色 |
| D、在新制氯水中滴加AgNO3溶液有白色沉淀生成 |
化学在人类生活中扮演着重要角色,以下应用不正确的是( )
| A、用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的 |
| B、浓硫酸具有吸水性,可用来干燥O2、Cl2、NH3等气体 |
| C、醋可用于除去暖水瓶中的水垢 |
| D、FeCl3可用来制印刷电路板 |
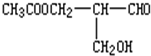 在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性.如图的物质有光学活性,发生下列反应后生成的有机物无光学活性的是( )
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”.凡有一个手性碳原子的物质一定具有光学活性.如图的物质有光学活性,发生下列反应后生成的有机物无光学活性的是( )