题目内容
 如图所示,在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气的成分仍不变.则钠和氧化汞的物质的量之比是( )
如图所示,在密闭容器中,一边装有一定量的金属钠,一边装有一定量的氧化汞,同时加热容器的两部分,钠和氧化汞都完全反应后,恢复到原温度,容器内空气的成分仍不变.则钠和氧化汞的物质的量之比是( )| A、1:1 |
| B、2:1 |
| C、23:216.6 |
| D、216.6:23 |
考点:钠的化学性质
专题:元素及其化合物
分析:完全反应后,恢复到原温度,容器中空气的成分仍不变,说明相当于钠和HgO发生置换反应生成过氧化钠和Hg,据此计算钠和HgO的物质的量之比.
解答:
解:完全反应后,恢复到原温度,容器中空气的成分仍不变,说明相当于钠和HgO发生置换反应生成过氧化钠和Hg,反应方程式为2Na+2HgO=Na2O2+2Hg,根据方程式知,Na和HgO的物质的量之比为1:1,故选A.
点评:本题以钠为载体考查根据方程式进行计算,正确书写方程式是解本题关键,注意:该过程中生成过氧化钠而不是氧化钠,为易错点.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
某温度下,向1L密闭容器中加入3mol A和2mol B发生反应:3A(g)+2B(l)═2C(g)+2D(g).5min后达到平衡,平衡时测得n(D)=1.8mol.下列说法错误的是( )
A、该反应的平衡常数表达式为K=
| ||
| B、反应前后压强不变,反应即达到平衡 | ||
| C、该反应达平衡时,A的转化率为90% | ||
| D、增加B的量,正反应速率增大,平衡正向移动 |
某有机物的结构简式为CH3CHClCH═CH-CHO,下列各项中,该有机物不可能发生的化学反应是( )
①氧化反应 ②取代反应 ③加成反应 ④消去反应 ⑤还原反应⑥酯化反应 ⑦水解反应 ⑧聚合反应.
①氧化反应 ②取代反应 ③加成反应 ④消去反应 ⑤还原反应⑥酯化反应 ⑦水解反应 ⑧聚合反应.
| A、② | B、④ | C、⑥ | D、⑧ |
用天平称量潮湿的或具有腐蚀性的药品时,药品必须放在( )
| A、托盘上 | B、纸上 |
| C、铁盒里 | D、玻璃器皿 |
下列选用的相关仪器符合实验要求的是( )
A、 存放浓硫酸 |
B、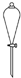 分离水和乙酸乙酯 |
C、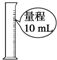 准确量取9.50mL |
D、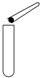 取金属颗粒 |
下列物质中,不属于合金的是( )
| A、硬铝 | B、黄铜 | C、钢铁 | D、金箔 |
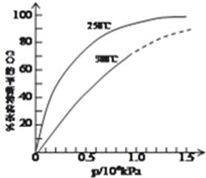 在容积可变的密闭容器中,由CO和H2合成甲醇CO(g)+2H2(g)═CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示.
在容积可变的密闭容器中,由CO和H2合成甲醇CO(g)+2H2(g)═CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示.